Udhëzuesi i fundit për bateritë
Udhëzuesi i mëposhtëm është shumë informues, kështu që ju lutemi gjeni atë që dëshironi të mësoni nga tabela e përmbajtjes në varësi të nivelit tuaj të njohurive të baterisë.Sigurisht nëse jeni fillestar, atëherë ju lutemi filloni në fillim.
Këshillë e para-leximit: Klikoni një herë në kutinë e tekstit të titullit dhe teksti i detajuar do të zgjerohet;Klikoni përsëri dhe teksti i detajuar do të fshihet.
Prezantimi
- Rëndësia dhe aplikimet e përhapura të baterive.
-
Bateritë janë shumë të rëndësishme në shoqërinë moderne dhe përdoren në një gamë të gjerë aplikimesh (me zhvillimin e teknologjisë, gjithnjë e më shumë pajisje po shndërrohen në energjinë e baterisë).Ato ofrojnë zgjidhje të lëvizshme, të rinovueshme dhe urgjente të energjisë që drejtojnë zhvillimin teknologjik, përdorimin e qëndrueshëm të energjisë dhe përparimin në një gamë të gjerë të industrive.

1 Pajisje elektronike portative: Siç janë telefonat mobil, tabletat, laptopët dhe kamerat dixhitale.
2 Transportim: Automjetet elektrike dhe hibride përdorin bateritë si pajisjen parësore të ruajtjes së energjisë.Me rritjen e kërkesës për energji të rinovueshme dhe mënyra të transportit miqësor me mjedisin, bateritë po luajnë një rol kryesor në drejtimin e zhvillimit të qëndrueshëm të transportit.
3 Ruajtje e energjisë së rinovueshme: Bateritë përdoren gjerësisht për të ruajtur burimet e energjisë së rinovueshme siç janë energjia diellore dhe e erës.Duke ruajtur energjinë elektrike në bateri, ato mund të sigurojnë një furnizim të qëndrueshëm të energjisë elektrike kur energjia diellore ose e erës nuk është e disponueshme.
4. Fuqi e urgjencës: Bateritë luajnë një rol të rëndësishëm si një burim i energjisë rezervë në situata urgjente.Për shembull, pajisje të tilla si telefona pa tel, pishtarë dhe dritat e urgjencës kërkojnë bateri të sigurojnë fuqi të besueshme.
5. Pajisje mjekësore: Shumë pajisje mjekësore, të tilla si pacemakers dhe ventilatorët artificialë, përdorin bateritë si një burim energjie.Stabiliteti dhe besueshmëria e baterive është thelbësore për funksionimin e këtyre pajisjeve kritike.
6. Aplikime ushtarake: Bateritë përdoren në një gamë të gjerë të aplikacioneve ushtarake, të tilla si për pajisjet e komunikimit ushtarak, sistemet e navigimit dhe dronët.Bateritë mund të sigurojnë një furnizim të pavarur me energji dhe të përmirësojnë aftësitë luftarake në fushën e betejës.
7 Industrial: Bateritë përdoren në industri për sistemet e baterive, furnizimet me energji urgjente dhe sensorët pa tel.Ato sigurojnë një furnizim të besueshëm të energjisë dhe sigurojnë vazhdimësinë dhe sigurinë e prodhimit industrial.
- Një përmbledhje e parimeve themelore dhe mekanizmave të punës të baterive.
-
Magjia e baterive qëndron në aftësinë e tyre për të kthyer energjinë kimike në energji elektrike.Një bateri përfshin dy elektroda (pozitive dhe negative) dhe një elektrolit.Elektroliti vepron si përcjellës i joneve, duke bërë të mundur një reaksion kimik midis elektrodave.
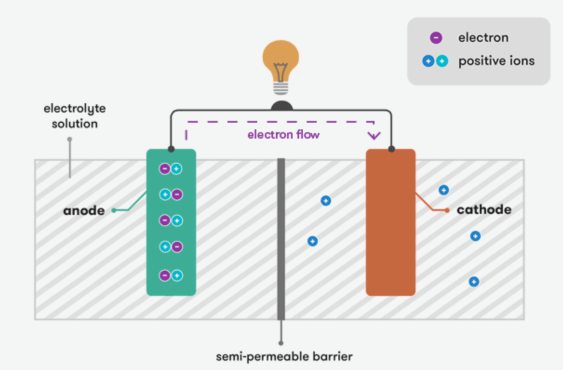
Parimi themelor i një baterie bazohet në reaksione elektrokimike.Kur ndodh një reaksion kimik, ai gjeneron rrjedhën e elektroneve.Në gjendjen e ngarkuar, bateria ruan kimikate midis elektrodave pozitive dhe negative, dhe reaksioni kimik është i kthyeshëm.Kur bateria është e lidhur me një qark të jashtëm, fillon reaksioni kimik, duke bërë që kimikati në terminalin pozitiv të oksidohet dhe kimikate në terminalin negativ për të zvogëluar.Si rezultat, elektronet rrjedhin nga terminali negativ në terminalin pozitiv, duke prodhuar një rrymë elektrike.Ky proces vazhdon derisa kimikatet të varfërohen.
Lloje të ndryshme të baterive përdorin reaksione të dallueshme kimike për të gjeneruar energji elektrike.Për shembull, lloji më i zakonshëm i baterisë litium-jon: elektroda e tij pozitive është e përbërë nga një përbërës litium (siç është oksidi i kobaltit ose fosfati i hekurit litium) dhe elektroda e tij negative është e përbërë nga një material karboni (siç është grafiti).Në gjendjen e ngarkuar, jonet e litiumit janë ngulitur nga elektroda pozitive në materialin negativ.Gjatë shkarkimit, jonet e litiumit janë të ngulitur nga elektroda negative dhe kthehen në elektrodën pozitive, duke lëshuar elektrone.
- Vlera e të pasurit një udhëzues përfundimtar për bateritë për lexuesit.
-
Një udhëzues përfundimtar është i vlefshëm për lexuesin për disa arsye:
1 Për të siguruar informacion të saktë: Interneti është plot me fragmente informacioni dhe mendime në kundërshtim.Një udhëzues përfundimtar ofron informacion gjithëpërfshirës dhe të saktë duke konsoliduar dhe mbledhur burime të besueshme për të ndihmuar lexuesit të përdorin shpejt njohuritë e nevojshme dhe të shmangin mashtrimet ose informacionin e pasaktë.
2 Kurseni kohë dhe përpjekje: Kërkimi i Internetit për tema specifike shpesh kërkon shumë kohë për të parë dhe verifikuar besueshmërinë e informacionit.Udhëzuesi Ultimate kursen kohë dhe përpjekje duke bashkuar informacione përkatëse në mënyrë që lexuesit të mund të gjejnë të gjitha informacionet që u duhen në një vend.
3 Zgjidhja e kontradiktave dhe konfuzionit: Interneti shpesh paraqet përgjigje të ndryshme për të njëjtën pyetje ose kontradikta midis informacionit.Udhëzuesi Ultimate ndihmon lexuesit të shpëtojnë nga konfuzioni dhe hutimi duke sintetizuar pikëpamje të ndryshme dhe burime autoritare për të dhënë përgjigjet më të besueshme.
4. Jepni udhëzime dhe këshilla: Udhëzuesi Ultimate jo vetëm që ofron fakte dhe informacione, por gjithashtu mund të sigurojë udhëzime dhe këshilla praktike.
- Lloje të ndryshme të baterive: parimet, karakteristikat dhe aplikimet.
-
Këtu janë disa nga 5 llojet më të zakonshme të baterive, përfshirë parimet, karakteristikat dhe aplikimet e tyre.Nëse dëshironi informacionin më gjithëpërfshirës për llojet e baterive, gjithashtu mund të kaloni këtë seksion dhe të shkoni direkt në "shumica e llojeve dhe aplikacioneve të baterive" më poshtë.
Bateri me acid
•Parimi: Bateritë e acidit plumb përdorin një reaksion kimik midis dioksidit të plumbit dhe plumbit për të prodhuar energji elektrike.
•Karakteristikat: Kostoja e ulët, dendësia e lartë e rrymës dhe e energjisë, por e madhe dhe e rëndë.
•Aplikimet: Bateritë fillestare të automobilave, UPS (furnizim me energji të pandërprerë), etj.
Bateritë li-jon (litium-jon)
•Parimi: Bateritë litium-jon përdorin migrimin e joneve litium midis elektrodave pozitive dhe negative për të ruajtur dhe lëshuar energji elektrike.
•Karakteristikat: Dendësia e lartë e energjisë, pesha më e lehtë dhe jeta e ciklit më të gjatë.Efikasitet i lartë i karikimit dhe shkarkimit.
•Aplikimet: Pajisjet mobile (p.sh. telefonat celularë, kompjuterët e tabletave), pajisjet elektronike portative dhe automjetet elektrike.
Bateritë NICD (Nickel-Cadmium)
•Parimi: Bateritë NICD prodhojnë energji elektrike përmes një reaksioni kimik midis nikelit dhe hidroksidit të kadmiumit.
•Karakteristikat: Prodhimi i fuqisë së lartë dhe jeta e gjatë, por ato përmbajnë kadmiumin e dëmshëm të metaleve të rënda, i cili ka një ndikim të caktuar në mjedis.
•Aplikimet: Kamerat dixhitale, mjetet e lëvizshme dhe dronët, etj.
Bateri hidride nimh (nikel-metal)
• Parimi: Bateritë NIMH përdorin reaksionin kimik midis nikelit dhe hidrogjenit për të ruajtur dhe lëshuar energji elektrike.
•Karakteristikat: Dendësia e lartë e energjisë, jeta e gjatë, pa ndotje dhe performancë më e mirë e temperaturës së lartë.
•Aplikimet: Automjete hibride, sisteme të ruajtjes së energjisë, etj.
Bateria lipo (litium polimer)

•Parimi: Bateria e polimerit litium është e ngjashme me baterinë e jonit litium, por përdor një elektrolit polimer të ngurtë në vend të një elektroliti të lëngshëm.
•Karakteristikat: Dendësia e lartë e energjisë, pesha më e lehtë, siguria më e mirë dhe niveli më i ulët i vetë-shkarkimit.I përshtatshëm për pajisjet e hollë.
•Aplikimet: Laptopët, orët e zgjuara dhe pajisjet mjekësore portative etj.
- Njohuri fizike për bateritë
- Tension (v)::
Tensioni paraqet ndryshimin e potencialit elektrik midis dy pikave në një qark.Matet në volt (V).Tensioni nëpër një bateri zakonisht shënohet si v_batt.
Ngarkoj (q):
Ngarkesa i referohet sasisë së ngarkesës elektrike të ruajtur në një bateri.Ajo matet në Coulombs (C) ose Ampere-Hours (AH).Marrëdhënia midis ngarkesës dhe kapacitetit jepet nga: Ngarkesa (Q) = Kapaciteti (C) × Tensioni (V)
Kapaciteti (c):
Kapaciteti përfaqëson sasinë e ngarkesës që një bateri mund të ruajë.Në mënyrë tipike matet në orët e amperës (AH) ose Milliamper-Hours (MAH).Marrëdhënia midis kapacitetit, ngarkimit dhe energjisë jepet nga: Energjia (E) = Kapaciteti (C) × Tensioni (V)
Energjia (e):
Energjia është aftësia për të bërë punë ose potenciali që një sistem të shkaktojë ndryshime.Në kontekstin e baterive, energjia shpesh matet në Watt-Hours (WH) ose Joules (J).Marrëdhënia midis energjisë, kapacitetit dhe ngarkesës jepet nga: Energjia (e) = ngarkesa (q) × tension (v)
Fuqia (P):
Fuqia përfaqëson shkallën në të cilën bëhet puna ose transferohet energjia.Ajo matet në vat (w).Fuqia në një qark llogaritet duke përdorur formulën: Fuqia (P) = Tensioni (V) × Rryma (I)
Seria Lidhja:
1. Kur bateritë janë të lidhura në seri, tensioni i përgjithshëm në të gjithë qark është shuma e tensioneve individuale të baterisë.Rryma mbetet e njëjtë.
Tensioni i përgjithshëm (v_total) = v1 + v2 + v3 + ...
2. Kur bateritë janë të lidhura në seri, kapaciteti total është shuma e kapaciteteve individuale të baterisë.Kjo për shkak se rryma mbetet e njëjtë, por tensioni i përgjithshëm rritet.
Kapaciteti total (C_TOTAL) = C1 + C2 + C3 + ...
Lidhje paralele:
1. Kur bateritë janë të lidhura paralelisht, tensioni i përgjithshëm mbetet i njëjtë me atë të një baterie individuale, ndërsa rryma totale është shuma e rrymave që rrjedhin përmes secilës bateri.
Rryma totale (i_total) = i1 + i2 + i3 + ...
2. Kur bateritë janë të lidhura paralelisht, kapaciteti i përgjithshëm është i barabartë me kapacitetin e një baterie të vetme.Kjo për shkak se tensioni mbetet i njëjtë, por rryma totale rritet.
Kapaciteti total (c_total) = c1 = c2 = c3 = ...
- Termat dhe përkufizimet e zakonshme të baterisë.
-
1 Kapaciteti i baterisë: Sasia e energjisë elektrike që një bateri mund të ruajë, e shprehur zakonisht në orët e ampit (AH) ose Milli-Amps (MAH).
2 Tension: Diferenca e mundshme ose diferenca e tensionit të një baterie, e shprehur në volt V. Ai përfaqëson sasinë e energjisë elektrike që bateria mund të ruajë.
3 Qelizë baterie: Një qelizë individuale në një bateri, që përmban elektrodën pozitive, elektrodën negative dhe elektrolitin.
4. Pako baterie: Një e tërë e përbërë nga disa qeliza të baterisë të kombinuara.Ata zakonisht janë të lidhur dhe menaxhuar përmes lidhësve, bordeve të qarkut dhe përbërësve të tjerë.
5. Seria Lidhja: Qeliza të shumta të baterive të lidhura në sekuencë, me terminalin pozitiv të lidhur me terminalin negativ, për të rritur tensionin e përgjithshëm.Kur lidhen në seri, voltazhet e qelizave janë mbivendosur.
6. Lidhje paralele: Lidh qelizat e shumta të baterive në sekuencë, me terminalin pozitiv të lidhur me terminalin negativ, për të rritur aftësinë totale të rrymës dhe kapacitetin.Kur lidhen paralelisht, kapacitetet e qelizave të baterisë shtohen së bashku.
7 Ngarkim: Ushqimi i energjisë elektrike në bateri nga një burim i jashtëm për të rivendosur energjinë kimike të ruajtur në bateri.
8. Shkarkim: Lëshimi i energjisë elektrike nga një bateri për përdorim në furnizimin e pajisjeve elektronike ose qarqeve.
9. Cikël: I referohet një procesi të plotë të karikimit dhe shkarkimit.
10. Efikasitet i ngarkimit: Raporti midis energjisë elektrike të zhytur nga bateria dhe energjia elektrike e ruajtur në të vërtetë gjatë procesit të karikimit.
11 Pa pagesë: Shkalla me të cilën një bateri humbet fuqinë më vete kur nuk është në përdorim.
12 Jetëgjatësi: Jetëgjatësia e një baterie, e matur zakonisht për sa i përket numrit të cikleve të ngarkimit ose kohës së përdorimit.
13 Jetëgjatësi: Sasia e kohës që një bateri mund të vazhdojë të furnizojë energjinë pas një ngarkese të vetme.
14 Karikim i shpejtë: Një teknologji e karikimit që i jep energji baterisë më shpejt për të zvogëluar kohën e karikimit.
15 Sistemi i Menaxhimit të Baterive (BMS): Një sistem elektrik që monitoron dhe kontrollon gjendjen e baterisë, procesin e karikimit dhe shkarkimit dhe mbron baterinë nga kushte të pafavorshme siç janë mbingarkesa dhe mbingarkesa.
16 Jeta e ciklit të baterive: Numri i cikleve të ngarkimit që një bateri mund të përfundojë, zakonisht e matur duke karikuar dhe shkarkuar në një humbje specifike të kapacitetit siç është 80% e kapacitetit origjinal.
17 Shkalla maksimale e ngarkimit: Shkalla maksimale e ngarkimit që mund të pranohet në mënyrë të sigurt nga bateria, e shprehur si një raport i kapacitetit të ngarkimit.
18 Shkalla maksimale e shkarkimit: Shkalla maksimale e rrymës me të cilën një bateri mund të shkarkohet në mënyrë të sigurt, të shprehet si raport i kapacitetit aktual.
19 Qark për mbrojtjen e baterive: Një pajisje sigurie e përdorur për të monitoruar gjendjen e baterisë dhe për të shkëputur qarkun e baterisë në rast të mbingarkesës, mbingarkesës, mbingarkesës, overtemperature, etj për të parandaluar dëmtimin ose rrezikun e baterisë.
20. Polaritet i baterisë: Dallimi dhe identifikimi midis terminaleve pozitive dhe negative të një baterie, të treguar zakonisht nga simbolet + dhe - ose shenjat.
21 Riciklimi i baterisë: Procesi i disponimit të baterive të përdorura për të rikuperuar dhe disponuar materialet e rrezikshme të përfshira në to dhe për të ripërdorur materialet e riciklueshme.
22 Shkarkim i thellë: Një gjendje në të cilën një bateri shkarkohet në një nivel shumë të ulët ose është varfëruar plotësisht.Shkarkimi i thellë zakonisht nuk rekomandohet shpesh për të shmangur efektet negative në jetën e baterisë.
23 Shkarkim i shpejtë: Një teknikë e shkarkimit që lëshon energjinë e baterisë në një rrymë të lartë për një periudhë të shkurtër kohe.
24. Dështim i baterisë: Një gjendje kur bateria nuk është në gjendje të sigurojë energji të mjaftueshme ose të mbajë funksionimin normal, i cili mund të shkaktohet nga arsye të ndryshme të tilla si plakja ose dëmtimi.
25 I arratisur termik : I referohet rritjes së shpejtë dhe të pakontrollueshme të temperaturës së një baterie në kushte jonormale, të tilla si mbingarkesa, mbingarkesa, mbinxehje, etj.
26. Elektroda baterie: Elektrodat pozitive dhe negative në një bateri, të cilat janë përbërësit kryesorë për ruajtjen dhe lëshimin e ngarkesës elektrike.
27 Stacion shkëmbimi i baterive: Një strukturë ose shërbim për zëvendësimin e shpejtë të baterive në automjetet elektrike për të siguruar një distancë më të gjatë.
28 Reaksion elektrokimik: Reagimi kimik që ndodh në një bateri për të kthyer energjinë kimike në energji elektrike përmes një procesi redoks.
29. Elektrolit: Një lëng përçues ose i ngurtë që përdoret për të transportuar jonet midis elektrodave pozitive dhe negative të një baterie për të lehtësuar reaksionin elektrokimik.
30. Ngarkues: Një pajisje për transferimin e energjisë elektrike në një bateri për të rivendosur energjinë e saj të ruajtur kimike.
31. Balancimi i baterisë: Një proces me të cilin është rregulluar niveli i ngarkesës ose shkarkimit të secilës qelizë në një paketë baterie për të siguruar që ngarkesa të jetë e ekuilibruar midis qelizave individuale.
32. Bateri e jashtme: Një njësi e heqshme e baterisë që mund të lidhet me një pajisje elektronike për të furnizuar me energji.
33. Treguesi i karikimit të baterisë: Një tregues ose ekran që tregon gjendjen e ngarkimit ose nivelin e një baterie.
34. Efekti i kujtesës së baterisë: Një fenomen me anë të së cilës kapaciteti i një baterie gradualisht zvogëlohet pasi ciklet e ngarkimit dhe shkarkimit përsëriten, pasi bateria kujton se vargjet më të vogla të ngarkimit dhe shkarkimit.
35. Rezistencë: I referohet rezistencës së brendshme të një baterie, e cila ndikon në efikasitetin dhe performancën e tij të konvertimit të energjisë.
36. Mbrojtje nga temperatura: Një funksion ose pajisje që monitoron dhe kontrollon temperaturën e një baterie për të parandaluar dëmtimin e mbinxehjes nëse temperatura bëhet shumë e lartë.
37. Mbrojtja e tensionit të ulët: Një mekanizëm mbrojtjeje që shkurton automatikisht qarkun për të parandaluar shkarkimin e tepërt kur tensioni i baterisë bie nën një prag të sigurt.
38. Mbrojtja e mbingarkuar: Një mekanizëm mbrojtjeje që automatikisht ndërpret qarkun për të parandaluar mbingarkesën kur ngarkesa e baterisë arrin pragun e sigurisë.
39. Ruajtje e baterisë: Procesi i mbajtjes së një baterie në një gjendje të papërdorur për një periudhë të zgjatur kohe, shpesh që kërkon masa të përshtatshme për të zvogëluar vetë-shkarkimin dhe për të mbrojtur baterinë.
40. Sistemi i Menaxhimit të Baterive (BMS): Një sistem elektronik për monitorimin, kontrollin dhe mbrojtjen e gjendjes dhe performancës së një pakete baterie, duke përfshirë menaxhimin e rrymës, tensionit, temperaturës dhe parametrave të tjerë.
41. Treguesi i nivelit të baterisë: Një pajisje ose funksion që tregon nivelin e ngarkesës që mbetet në një bateri, zakonisht shprehet si përqindje ose në disa faza.
42. Koha e karikimit: Koha e nevojshme për të sjellë një bateri nga një ngarkesë e ulët në një ngarkesë të plotë, e cila ndikohet nga fuqia e ngarkuesit dhe kapaciteti i baterisë.
43. Koeficient i temperaturës: Marrëdhënia midis performancës së baterisë dhe ndryshimeve në temperaturë, të cilat mund të ndikojnë në kapacitetin, rezistencën e brendshme dhe karakteristikat e ngarkimit/shkarkimit të baterisë.
44. Garancia e baterisë: Garancia e një prodhuesi për performancën dhe cilësinë e një baterie për një periudhë të caktuar kohe, e shprehur zakonisht në muaj ose vite.
45. Stacion mbushjeje: Një pajisje ose një strukturë e përdorur për të furnizuar automjete elektrike ose pajisje të tjera të baterisë për karikim.
46. Testues i baterisë: Një pajisje ose instrument i përdorur për të matur tensionin, kapacitetin, rezistencën e brendshme dhe parametrat e tjerë të një baterie për të vlerësuar shëndetin dhe performancën e tij.
47. Balancimi aktiv: Një teknikë e menaxhimit të baterisë që barazon ngarkesën në një paketë baterie duke kontrolluar nivelin e ngarkesës dhe shkarkimit midis qelizave individuale.
48. Balancim pasiv: Një teknikë e menaxhimit të baterisë në të cilën ngarkesa në një paketë baterie është e ekuilibruar duke lidhur rezistorë ose rrjedhje të ngarkesës, zakonisht më pak efikase sesa balancimi aktiv.
49. Paketim baterie : Paketimi i jashtëm i një baterie, i përdorur për të mbrojtur qelizën, për të siguruar mbështetje strukturore dhe për të parandaluar qarqet e shkurtra.
50. Densitet i lartë i energjisë: Sasia maksimale e energjisë elektrike që një bateri mund të ruajë për vëllimin ose peshën e njësisë, duke treguar efikasitetin e ruajtjes së energjisë së baterisë.
51. Shkalla e ulët e vetë-shkarkimit: Shkalla me të cilën një bateri humbet energjinë elektrike në vetvete është shumë e ngadaltë dhe mban një gjendje të lartë të ngarkuar kur ruhet ose i papërdorur për një periudhë të gjatë kohore.
52. Polarizimi i baterisë: I referohet ndryshimit të materialit në sipërfaqen e elektrodave gjatë karikimit dhe shkarkimit për shkak të reaksioneve kimike në elektroda.
53. Rrjedhje e elektrolitit të baterisë: Një gjendje në të cilën elektroliti në një bateri rrjedh në mjedisin e jashtëm, i cili do të rezultojë në degradimin e performancës së baterisë ose problemeve të tjera të sigurisë.
54. Sistemi i ftohjes së baterisë: Një sistem i përdorur për të kontrolluar temperaturën e një baterie, qoftë përmes shpërndarjes së nxehtësisë, tifozit ose ftohjes së lëngshme për të mbajtur baterinë brenda intervalit të duhur të temperaturës së funksionimit.
55. Sistemi i ngrohjes së baterive: Një sistem i përdorur për të siguruar nxehtësi në bateri në mjedise me temperaturë të ulët për të siguruar funksionimin e duhur të baterisë në temperatura të ulëta.
56. Bateria e nivelit të lartë të shkarkimit: Një bateri që është e aftë të sigurojë energji elektrike në një rrymë të lartë për aplikime me kërkesa të larta të energjisë siç janë mjetet e energjisë dhe automjetet elektrike.
57. Bateri sekondare: Një bateri që mund të rimbushet, në krahasim me një bateri të disponueshme që nuk mund të rimbushet.
58. Monitor i baterisë: Një pajisje ose sistem për monitorimin e statusit, tensionit, temperaturës dhe parametrave të tjerë të një baterie në kohë reale për të siguruar informacion dhe për të mbrojtur baterinë.
- Ndërtimi i baterisë: elektroda, elektrolit dhe ndarës.
-
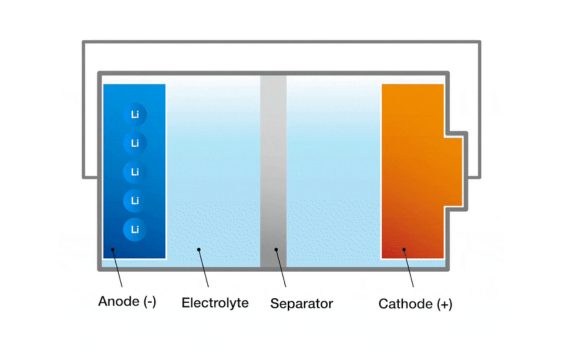
1 Elektrodë: Elektrodat në një bateri ndahen në një elektrodë pozitive dhe një negative.Elektroda pozitive është aty ku reaksioni i oksidimit zhvillohet në bateri dhe elektroda negative është aty ku reaksioni i zvogëlimit zhvillohet në bateri.Elektrodat pozitive dhe negative përbëhen nga materiale përçuese, zakonisht përdoren metale, karbon ose komponime.Dallimi në potencial midis elektrodave pozitive dhe negative prodhon tensionin e qelizës së baterisë.
2 Elektrolit: Elektroliti është mediumi midis elektrodave i cili lejon që jonet të kalojnë midis elektrodave dhe mban ekuilibrin e ngarkimit.Elektroliti mund të jetë në formë të lëngshme, të ngurtë ose xhel, në varësi të llojit të qelizës.Në një qelizë të lëngshme, elektroliti është zakonisht një përbërës jonik i tretur në tretësirë.
3 Diafragmë: Diafragma është një pengesë fizike midis elektrodave pozitive dhe negative, duke parandaluar rrjedhën e drejtpërdrejtë të elektroneve, por duke lejuar që jonet të kalojnë.Funksioni i diafragmës është të parandalojë qarkullimin e shkurtër të elektrodave pozitive dhe negative ndërsa lejon jonet të lëvizin lirshëm përmes elektrolitit dhe të ruajnë ekuilibrin e ngarkimit të qelizës.Diafragma zakonisht është bërë nga një material polimer ose një material qeramik.
Këto përbërës punojnë së bashku për të formuar strukturën e qelizës së baterisë.
- Proceset e ngarkimit dhe shkarkimit në bateri: reaksione kimike dhe rrjedhë e rrymës.
-
1 Proces i shkarkimit: Kur shkarkohet një bateri, energjia kimike shndërrohet në energji elektrike.Gjatë shkarkimit, një reaksion oksidimi bëhet në terminalin pozitiv dhe një reagim zvogëlimi në terminalin negativ.Reagimet kimike prodhojnë elektrone dhe jone.Elektroda pozitive lëshon elektrone, të cilat rrjedhin përmes një qarku të jashtëm për të prodhuar një rrymë elektrike.Elektroda negative merr elektrone, të cilat kombinohen me jonet për të formuar komponime.Në të njëjtën kohë, jonet lëvizin nëpër elektrolit, duke ruajtur bilancin e ngarkimit të baterisë.
2Proces i ngarkimit: Gjatë karikimit të një baterie, energjia elektrike shndërrohet në energji kimike në mënyrë që të ruajë energjinë.Gjatë procesit të karikimit, një burim i jashtëm i energjisë aplikon një tension përpara, duke bërë që një rrymë të kalojë nëpër bateri.Tensioni pozitiv ndryshon baterinë dhe ndryshon reaksionin kimik midis elektrodave pozitive dhe negative.Elektroda pozitive pranon elektrone dhe elektroda negative i lëshon ato.Reagimi kimik ruan energjinë elektrike si energji potenciale kimike, duke rikthyer baterinë në gjendjen e saj origjinale.Jonet lëvizin nëpër elektrolit për të ruajtur ekuilibrin e ngarkesës.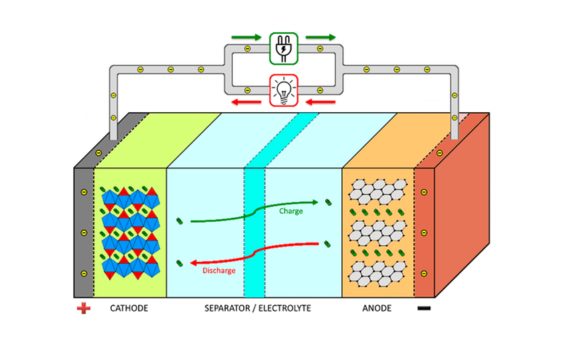
- Tensioni i baterisë, kapaciteti dhe dendësia e energjisë.
-
Tensioni:
Tensioni është një masë e forcës së daljes elektrike të një baterie.Zakonisht shprehet në volt.Tensionet e zakonshme të qelizave të baterisë janë si më poshtë:
•Bateria litium-jon (Li-jon): Në përgjithësi 3.6 volt në 3.7 volt.Ajo që është më e veçantë është se bateria LifePo4 (fosfati i hekurit litium) është 3.2 volt.(Tensioni i vetëm i qelizave)
•Bateria e nikelit-cadmium (NICD): 1.2 volt (tension me një qelizë).
•NenHidride ickel-metalike (NIMH): 1.2 volt (tension me një qelizë).
•Bateria e acidit plumb (acid plumbi): 2 volt në 2.2 volt (tension i vetëm qelizor).Bateritë e acidit plumb përdoren zakonisht në fillimin e automobilave, sistemet e ruajtjes së energjisë dhe fushat e tjera.
•Bateria zink-alkaline (zink-karbon): 1.5 volt (tension me një qelizë).Ky lloj i baterisë zakonisht gjendet në bateritë alkaline me përdorim të vetëm si bateritë AA dhe AAA.
Më sipër janë tensionet e baterive të ndryshme, dhe ne gjithashtu mund të rrisim tensionin duke i lidhur ato në seri.Shembuj janë si më poshtë:
•Tre bateri 3.7V litium-jon janë të lidhura në seri për të marrë një paketë baterie litium-jon 11.1V (d.m.th., ajo që ne shpesh e quajmë një paketë baterie litium-jon 12V);
•Tre bateri 2V me acid plumbi janë të lidhura në seri për të marrë një paketë baterie të acidit të plumbit 6V;
• Katër bateri fosfati prej hekuri litium 3.2V janë të lidhura në seri për të marrë një paketë baterie fosfati të hekurit litium 12.8V (d.m.th., atë që ne shpesh e quajmë një paketë baterie fosfati prej hekuri litium 12V)
Kapaciteti
Kur flasim për kapacitetin e baterisë, shpesh shprehet duke përdorur njësinë e orëve të amperës (AH) ose Milliamper-Hours (MAH).Kapaciteti i baterisë është sasia e ngarkesës që një bateri mund të ruajë dhe gjithashtu mund të kuptohet si produkt i rrymës dhe kohës që bateria mund të japë.Këtu janë disa shifra shembulli dhe mënyra se si përshkruhen:
•Bateria 2000 mAh: Kjo do të thotë që bateria ka një kapacitet prej 2000 mAh.Nëse pajisja tërheq një rrymë mesatare prej 200 milliamps (MA) në orë, atëherë kjo bateri mund të furnizojë teorikisht energji për 10 orë (2000mAh / 200MA = 10 orë).
•Bateria 5AH: Kjo do të thotë që bateria ka një kapacitet prej 5 orësh amp.Nëse pajisja konsumon një rrymë mesatare prej 1 amp (a) në orë, atëherë kjo bateri mund të fuqizojë teorikisht për 5 orë (5AH / 1A = 5 orë).
Paketat e baterisë mund të lidhen paralelisht për të dhënë një kapacitet të rritur, për shembull:
•2 bateri Li-jon e 12V-100AH mund të lidhen paralelisht për të marrë një paketë baterie Li-jon prej 12V-200AH.
•2 bateri LifePo4 prej 3.2V-10AH mund të lidhen paralelisht për të marrë një paketë baterie LIFEPO4 prej 3.2V-20AH.
Karikuesi i baterisë 1000mAh: Ky është një karikues që mund të ngarkojë baterinë me një normë prej 1000 miliampe (MA) në orë.Nëse keni një bateri 2000mAh, duke e ngarkuar atë me këtë karikues teorikisht do të zgjasë 2 orë (2000mAh / 1000mA = 2 orë) për ta ngarkuar plotësisht atë.
Në praktikë, koha e llogaritur teorikisht e përdorimit të baterisë mund të devijojë për shkak të veshjes së baterisë dhe lotave dhe faktorëve të tjerë.
Dendësia e energjisë:
Dendësia e energjisë është një masë e efikasitetit të energjisë së ruajtur në një bateri.Ai tregon sasinë e energjisë që mund të ruhet për vëllimin e njësisë ose peshën njësi të baterisë.Njësitë e zakonshme të densitetit të energjisë janë vat-orë për kilogram (WH/kg) ose vat-orë për litër (WH/L).
•Bateria litium-jon: Bateritë litium-jon kanë densitet të lartë të energjisë, që zakonisht variojnë nga 150 deri në 250 WH/kg.
•Bateria NIMH: Bateritë NIMH kanë një densitet më të ulët të energjisë në krahasim me bateritë litium-jon.Ato zakonisht variojnë nga 60 deri në 120 WH/kg.
•Bateria e acidit plumbi: Bateritë e acidit plumb kanë densitet relativisht të ulët të energjisë në krahasim me bateritë litium-jon.Ato zakonisht variojnë nga 30 deri në 50 wh/kg.
•Bateria e zinkut-karbonit: Bateritë e zinkut-karbonit kanë densitet më të ulët të energjisë në krahasim me bateritë litium-jon.Ato zakonisht variojnë nga 25 deri në 40 WH/kg.
- Rekomandime për ruajtjen e baterisë
-
Ruajtja e duhur e baterisë është thelbësore për të ruajtur shëndetin e baterisë dhe për të zgjatur jetëgjatësinë e saj.Këtu janë disa rekomandime për ruajtjen e baterive:
•Temperatura: Ruani bateritë në një vend të freskët dhe të thatë me një temperaturë midis 15 ° C dhe 25 ° C (59 ° F dhe 77 ° F).Temperaturat e larta mund të përshpejtojnë normën e vetë-shkarkimit dhe të shkurtojnë jetën e raftit të baterisë.Shmangni ekspozimin e baterive në nxehtësi ekstreme ose të ftohtë.
•Shmangni lagështinë: lagështia mund të dëmtojë bateritë, duke çuar në gërryerje ose rrjedhje.Mbajini bateritë larg mjediseve të lagështa, të tilla si bodrumet ose banjat.Sigurohuni që zona e ruajtjes të jetë e thatë dhe e ajrosur mirë.
•Niveli i ngarkimit: Para se të ruani bateritë për një periudhë të zgjatur, është më mirë të siguroheni që ato janë pjesërisht të ngarkuara.Shumica e prodhuesve rekomandojnë një nivel ngarkimi prej rreth 40% deri 60% për ruajtje afatgjatë.Kjo diapazon ndihmon në parandalimin e kushteve të tepërta ose të mbingarkesës gjatë ruajtjes.
•Lloji i baterisë: Kimistritë e ndryshme të baterisë kanë kërkesa specifike të ruajtjes.Këtu janë disa udhëzime për llojet e zakonshme:
a Bateritë alkaline: Bateritë alkaline kanë një jetë të gjatë rafti dhe mund të ruhen për disa vjet.Ato nuk janë të rimbushshme dhe nuk duhet të ekspozohen ndaj temperaturave ekstreme.
b. Bateritë litium-jon: Bateritë Li-jon zakonisht elektronikë të lëvizshëm me energji elektrike.Nëse planifikoni t'i ruani ato për një periudhë të zgjatur, synoni një nivel ngarkimi midis 40% dhe 60%.Shmangni ruajtjen e baterive Li-jon me ngarkesë të plotë ose shkarkuar plotësisht.
c. Bateritë e acidit plumbi: Këto zakonisht përdoren në automjete dhe sistemet rezervë të energjisë.Për ruajtje afatgjatë, mbajini bateritë e acidenit plumb të ngarkuar plotësisht.Kontrolloni rregullisht nivelet e elektrolitit dhe ngjiteni me ujë të distiluar nëse është e nevojshme.
d. Bateritë me bazë nikeli (NIMH dhe NICD): Bateritë NIMH dhe NICD duhet të ruhen me një ngarkesë të pjesshme (rreth 40%).Nëse ata shkarkohen plotësisht para ruajtjes, ata mund të zhvillojnë depresion të tensionit, duke zvogëluar kapacitetin e tyre të përgjithshëm.
•GocëRuajtja e Eparatit: Ruani bateritë në një mënyrë që parandalon kontaktin midis terminaleve të tyre.Nëse terminalet pozitive dhe negative prekin njëri -tjetrin ose vijnë në kontakt me materiale përçuese, mund të shkaktojë shkarkim dhe dëmtim të mundshëm.
•Paketimi origjinal: Paketimi origjinal është krijuar për të mbrojtur bateritë nga lagështia, pluhuri dhe ndotësit e tjerë.
•Inspektimi i rregullt: Inspektoni në mënyrë periodike bateritë e ruajtura për çdo shenjë të rrjedhjes, gërryerjes ose dëmtimit.Nëse vini re ndonjë problem, trajtojini ato me kujdes dhe hidhni ato siç duhet.
- Ndikim mjedisor.
-
Riciklimi i baterisë: Bateritë përmbajnë kimikate dhe metale të ndryshme që mund të jenë të dëmshme për mjedisin nëse nuk hidhen siç duhet.Bateritë e riciklimit ndihmojnë në rikuperimin e materialeve të vlefshme si litium, kobalt dhe nikel, dhe parandalon lëshimin e substancave toksike.Shumë komunitete kanë programe të riciklimit të baterive ose vendndodhje të braktisjes.Kontrolloni me autoritetet lokale ose qendrat e riciklimit për të gjetur opsionet e duhura të asgjësimit në zonën tuaj.
Substanca të rrezikshme: Disa bateri, të tilla si bateritë e acidit plumb të përdorura në automjete, përmbajnë substanca të rrezikshme si plumbi dhe acidi sulfurik.Hedhja e pahijshme e këtyre baterive mund të kontaminojë burimet e tokës dhe ujit, duke paraqitur një rrezik për shëndetin e njeriut dhe mjedisin.Ndërsa njerëzit bëhen më të vetëdijshëm për mbrojtjen e mjedisit, gjithnjë e më shumë njerëz përdorin bateri më miqësore me mjedisin litium-jon, veçanërisht bateritë LifePo4.
Konsumim i energjise: Prodhimi i baterisë kërkon energji, dhe ndikimi mjedisor ndryshon në varësi të llojit të baterisë.Për shembull, prodhimi i baterive litium-jon të përdorura në shumë pajisje elektronike dhe automjete elektrike përfshin nxjerrjen dhe përpunimin e mineraleve.Përdorimi i pajisjeve me efikasitet energjetik dhe optimizimi i përdorimit të baterisë mund të ndihmojë në uljen e konsumit të përgjithshëm të energjisë.
Gjurmë të karbonit: Gjurma e karbonit e lidhur me prodhimin dhe asgjësimin e baterisë mund të kontribuojë në emetimet e gazrave serë dhe ndryshimin e klimës.Miratimi i rritur i burimeve të rinovueshme të energjisë për prodhimin dhe riciklimin e baterive mund të ndihmojë në zbutjen e ndikimit në mjedis.