Канчатковае кіраўніцтва па батарэях
Наступнае кіраўніцтва вельмі інфарматыўнае, таму, калі ласка, знайдзіце тое, што вы хочаце даведацца з зместу ў залежнасці ад узроўню ведаў пра батарэі.Зразумела, калі вы пачатковец, то, калі ласка, пачніце ў пачатку.
Папярэдняе чытанне савета: Націсніце адзін раз на загалоўным тэкставым полі, і падрабязны тэкст пашырыцца;Націсніце яшчэ раз, і падрабязны тэкст будзе схаваны.
Уводзіны
- Важнасць і шырокае прымяненне батарэй.
-
Батарэі вельмі важныя ў сучасным грамадстве і выкарыстоўваюцца ў шырокім дыяпазоне прыкладанняў (пры распрацоўцы тэхналогій усё больш і больш прылад пераўтвараюцца ў магутнасць батарэі).Яны забяспечваюць партатыўныя, аднаўляльныя і аварыйныя сілавыя рашэнні, якія абумоўліваюць тэхналагічнае развіццё, устойлівае выкарыстанне энергіі і прагрэс у шырокім дыяпазоне галін.

1. Партатыўныя электронныя прылады: Напрыклад, мабільныя тэлефоны, планшэты, ноўтбукі і лічбавыя камеры.
2. Перавозка: Электрычныя і гібрыдныя транспартныя сродкі выкарыстоўваюць батарэі ў якасці прылады для захоўвання асноўнай энергіі.З павелічэннем попыту на аднаўляльныя крыніцы энергіі і экалагічна чыстых спосабаў транспарту батарэі гуляюць ключавую ролю ў кіраванні ўстойлівым развіццём транспарту.
3. Аднаўляльныя крыніцы энергіі: Батарэі шырока выкарыстоўваюцца для захоўвання аднаўляльных крыніц энергіі, такіх як сонечная і ветравая энергія.Захоўваючы электрычную энергію ў батарэях, яны могуць забяспечыць пастаяннае харчаванне электраэнергіі, калі сонечная і ветравая энергія недаступна.
4. Аварыйная магутнасць: Батарэі гуляюць важную ролю як рэзервовую крыніцу магутнасці ў экстраных сітуацыях.Напрыклад, такія прылады, як бесправадныя тэлефоны, паходні і аварыйныя ліхтары, патрабуюць батарэй, каб забяспечыць надзейную магутнасць.
5. Медыцынскае абсталяванне: Многія медыцынскія прылады, такія як кардыёстымулятары і штучныя вентылятары, выкарыстоўваюць батарэі ў якасці крыніцы харчавання.Устойлівасць і надзейнасць батарэй маюць вырашальнае значэнне для працы гэтых крытычных прылад.
6. Ваенныя прыкладанні: Батарэі выкарыстоўваюцца ў шырокім дыяпазоне ваенных прыкладанняў, напрыклад, для абсталявання ваеннай камунікацыі, навігацыйных сістэм і беспілотнікаў.Батарэі могуць забяспечыць незалежнае харчаванне энергіі і пашыраць баявыя магчымасці на полі бою.
7. Індустрыяльны: Акумулятары выкарыстоўваюцца ў прамысловасці для сістэм батарэі, аварыйных электразабеспячэння і бесправадных датчыкаў.Яны забяспечваюць надзейнае харчаванне і забяспечваюць пераемнасць і бяспеку прамысловай вытворчасці.
- Агляд асноўных прынцыпаў і механізмаў працы батарэй.
-
Магія батарэй заключаецца ў іх здольнасці пераўтвараць хімічную энергію ў электрычную энергію.Акумулятар складаецца з двух электродаў (станоўчых і адмоўных) і электраліта.Электраліт дзейнічае як правадыр іёнаў, што дазваляе хімічнай рэакцыяй паміж электродамі.
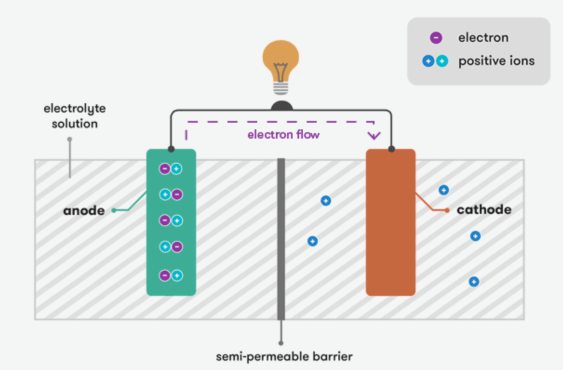
Прынцыповы прынцып батарэі заснаваны на электрахімічных рэакцыях.Калі ўзнікае хімічная рэакцыя, яна стварае паток электронаў.У зараджаным стане акумулятар захоўвае хімічныя рэчывы паміж станоўчымі і адмоўнымі электродамі, а хімічная рэакцыя зварачальная.Калі акумулятар падключаецца да знешняй схемы, пачынаецца хімічная рэакцыя, што выклікае хімічнае рэчыва пры станоўчым тэрмінале для акіслення і хімічнага рэчыва пры адмоўным тэрмінале для памяншэння.У выніку электроны перацякаюць ад адмоўнага тэрмінала да станоўчага тэрмінала, ствараючы электрычны ток.Гэты працэс працягваецца, пакуль хімічныя рэчывы не будуць вычарпаны.
У розных тыпах батарэй выкарыстоўваюцца розныя хімічныя рэакцыі для атрымання электраэнергіі.Напрыклад, найбольш распаўсюджаны тып літый-іённай батарэі: яго станоўчы электрод складаецца з літыя злучэння (напрыклад, аксід кобальту або фасфат літыя), а яго адмоўны электрод складаецца з вугляроднага матэрыялу (напрыклад, графіту).У зараджаным стане іёны літыя ўбудаваны з станоўчага электрода ў адмоўны матэрыял.Падчас выпіскі іёны літыя дэ-убудаваны з адмоўнага электрода і вяртаюцца ў станоўчы электрод, вылучаючы электроны.
- Значэнне наяўнасці канчатковага кіраўніцтва па батарэях для чытачоў.
-
Канчатковае кіраўніцтва з'яўляецца каштоўным для чытача па некалькіх прычынах:
1. Каб забяспечыць дакладную інфармацыю: Інтэрнэт поўны фрагментаў інфармацыі і супярэчлівых меркаванняў.Канчатковае кіраўніцтва дае вычарпальную і дакладную інфармацыю, кансалідуючы і збіраючы надзейныя крыніцы, каб дапамагчы чытачам хутка атрымаць доступ да неабходных ведаў, і пазбягаць уводзіць у зман або няправільную інфармацыю.
2. Зэканомце час і намаганні: Пошук у Інтэрнэце па пэўных тэмах часта патрабуе вялікага часу, каб прасейваць і праверыць надзейнасць інфармацыі.Канчатковае кіраўніцтва эканоміць час і намаганні, аб'ядноўваючы адпаведную інфармацыю, каб чытачы маглі знайсці ўсю неабходную інфармацыю ў адным месцы.
3. Вырашэнне супярэчнасцей і разгубленасці: Інтэрнэт часта ўяўляе розныя адказы на адно і тое ж пытанне ці супярэчнасці паміж інфармацыяй.Канчатковае кіраўніцтва дапамагае чытачам пазбегнуць блытаніны і здзіўлення, сінтэзуючы розныя погляды і аўтарытэтныя крыніцы, каб даць самыя надзейныя адказы.
4. Прадаставіць рэкамендацыі і парады: Канчатковае кіраўніцтва не толькі дае факты і інфармацыю, але і можа даць практычныя рэкамендацыі і парады.
- Розныя тыпы батарэй: прынцыпы, характарыстыкі і прыкладанні.
-
Вось некаторыя з 5 найбольш распаўсюджаных тыпаў батарэй, у тым ліку іх прынцыпы, характарыстыкі і прыкладанні.Калі вы хочаце найбольш поўную інфармацыю пра тыпы батарэі, вы таксама можаце прапусціць гэты раздзел і перайсці да "Большасць тыпаў і прыкладанняў батарэі" ніжэй.
Свінцова-кіслотныя батарэі
•Прынцып: батарэі свінцова-кіслотнага рэжыму выкарыстоўваюць хімічную рэакцыю паміж дыяксідам свінцу і свінцу для атрымання электрычнай энергіі.
•Асаблівасці: нізкая кошт, высокая шчыльнасць току і энергіі, але вялікая і цяжкая.
•Прыкладанні: Аўтамабільныя стартавыя батарэі, ІБП (бесперабойнае харчаванне) і г.д.
Літы-іённыя (літый-іённыя) батарэі
•Прынцып: літый-іённыя батарэі выкарыстоўваюць міграцыю іёнаў літыя паміж станоўчымі і адмоўнымі электродамі для захоўвання і вызвалення электрычнай энергіі.
•Асаблівасці: высокая шчыльнасць энергіі, больш лёгкая вага і працяглы тэрмін службы цыкла.Высокая эфектыўнасць зарадкі і разраду.
•Прыкладанні: мабільныя прылады (напрыклад, мабільныя тэлефоны, планшэтныя кампутары), партатыўныя электронныя прылады і электрамабілі.
Батарэі NICD (нікель-кадмій)
•Прынцып: батарэі NICD вырабляюць электрычную энергію праз хімічную рэакцыю паміж нікелем і гідраксідам кадмію.
•Асаблівасці: Выхад з высокай магутнасцю і доўгае жыццё, але яны ўтрымліваюць шкодны кадмій хэві -металу, які аказвае пэўны ўплыў на навакольнае асяроддзе.
•Прыкладанні: лічбавыя камеры, партатыўныя інструменты і беспілотнікі і г.д.
NIMH (нікель-метал) гідрыдныя батарэі
• Прынцып: батарэі NIMH выкарыстоўваюць хімічную рэакцыю паміж нікелем і вадародам для захоўвання і вылучэння электрычнай энергіі.
•Асаблівасці: высокая шчыльнасць энергіі, доўгае жыццё, не забруджванне і больш высокія высокія тэмпературныя характарыстыкі.
•Прыкладанні: гібрыдныя транспартныя сродкі, сістэмы захоўвання энергіі і г.д.
Акумулятар ліпа (палімер літыя)

•Прынцып: літый -палімерная батарэя падобная на літый -іённую батарэю, але ён выкарыстоўвае цвёрды палімерны электраліт замест вадкага электраліта.
•Асаблівасці: высокая шчыльнасць энергіі, больш лёгкая вага, лепшая бяспека і зніжэнне ўзроўню самаадчування.Падыходзіць для тонкіх прылад.
•Прыкладанні: ноўтбукі, разумныя гадзіны і партатыўныя медыцынскія прылады і г.д.
- Фізіка Веданне батарэй
- Напружанне (v):
Напружанне ўяўляе сабой розніцу электрычнага патэнцыялу паміж двума кропкамі ў ланцугу.Ён вымяраецца ў вольтах (V).Напружанне ў батарэі звычайна абазначаецца як v_batt.
Зарад (Q):
Зарад ставіцца да колькасці электрычнага зарада, які захоўваецца ў батарэі.Ён вымяраецца ў кулонах (С) або ампер-гадзінах (AH).Узаемасувязь паміж зарадам і магутнасцю задаецца: Зарад (Q) = ёмістасць (C) × напружанне (v)
Ёмістасць (C):
Ёмістасць уяўляе колькасць зарадкі, якую батарэя можа захоўваць.Звычайна ён вымяраецца ў ампер-гадзінах (AH) або Milliampere-Hours (MAH).Узаемасувязь паміж магутнасцю, зарадам і энергіяй задаецца: Энергія (E) = ёмістасць (C) × напружанне (V)
Энергія (е):
Энергія - гэта здольнасць выконваць працу альбо патэнцыял для сістэмы, каб выклікаць змены.У кантэксце батарэй энергія часта вымяраецца ў ват-гадзінах (WH) або Joules (J).Узаемасувязь паміж энергіяй, ёмістасцю і зарадам задаецца: Энергія (E) = зарад (Q) × напружанне (V)
Магутнасць (P):
Магутнасць уяўляе сабой хуткасць, з якой ажыццяўляецца праца, альбо перадаецца энергія.Ён вымяраецца ў ват (w).Магутнасць у ланцугу разлічваецца пры дапамозе формулы: Магутнасць (P) = напружанне (v) × ток (i)
Падключэнне да серыі:
1. Калі батарэі злучаюцца паслядоўна, агульнае напружанне па ланцугу - гэта сума асобных напружанняў батарэі.Ток застаецца ранейшым.
Агульнае напружанне (V_Total) = V1 + V2 + V3 + ...
2. Калі батарэі падключаюцца паслядоўна, агульная ёмістасць - гэта сума асобных ёмістасцей батарэі.Гэта таму, што ток застаецца ранейшым, але агульнае напружанне павялічваецца.
Агульная ёмістасць (C_Total) = C1 + C2 + C3 + ...
Паралельнае злучэнне:
1. Калі батарэі падключаюцца паралельна, агульнае напружанне застаецца такім жа, як у асобнай батарэі, у той час як агульны ток - гэта сума токаў, якія праходзяць праз кожную батарэю.
Агульны ток (i_total) = i1 + i2 + i3 + ...
2. Калі батарэі падключаюцца паралельна, агульная ёмістасць роўная ёмістасці адной батарэі.Гэта таму, што напружанне застаецца ранейшым, але агульны ток павялічваецца.
Агульная ёмістасць (C_Total) = C1 = C2 = C3 = ...
- Агульныя тэрміны і азначэнні батарэі.
-
1. Акумулятар ёмістасць: Колькасць электрычнай энергіі, якую можа захоўваць акумулятар, звычайна выражаецца ў AMP-гадзінах (AH) або Milli-Amps (MAH).
2. Напружанне: Розніца ў патэнцыяле або розніца напружання батарэі, выражаная ў вольце V. Гэта ўяўляе колькасць электрычнай энергіі, якую батарэя можа захоўваць.
3. Ячэйка батарэі: Асобная клетка ў батарэі, якая змяшчае станоўчы электрод, адмоўны электрод і электраліт.
4. Акумулятарная батарэя: Цэлае, якое складаецца з некалькіх клетак батарэі ў спалучэнні.Звычайна яны падключаюцца і кіруюцца праз раздымы, дошкі і іншыя кампаненты.
5. Падключэнне да серыі: Шматразовыя клеткі батарэі, падлучаныя паслядоўна, з станоўчым тэрміналам, падключаным да адмоўнага тэрмінала, для павелічэння агульнага напружання.Пры падключэнні паслядоўна напружанне клетак накладваецца.
6. Паралельнае злучэнне: Падключае некалькі вочак батарэі паслядоўна, з станоўчым тэрміналам, падключаным да адмоўнага тэрмінала, для павелічэння агульнай магчымасці току і магутнасці.Пры падключэнні паралельна ёмістасць акумулятарных клетак дадаецца разам.
7. Зарадка: Кармленне электрычнай энергіі ў батарэю з знешняй крыніцы для аднаўлення хімічнай энергіі, якая захоўваецца ў батарэі.
8. Выкід: Выпуск электрычнай энергіі з батарэі для выкарыстання ў пастаўцы электроннага абсталявання або схем.
9. Цыкл зарада: Ставіцца да поўнага працэсу зарадкі і разраду.
10. Эфектыўнасць зарадкі: Суадносіны паміж электрычнай энергіяй, паглынутай батарэяй, і электрычнай энергіяй, фактычна захоўваецца падчас працэсу зарадкі.
11. Самаразраванне: Хуткасць, з якой батарэя губляе магутнасць самастойна, калі не выкарыстоўваецца.
12. Тэрмін службы батарэі: Тэрмін службы батарэі, які звычайна вымяраецца з пункту гледжання колькасці цыклаў зарадкі або часу выкарыстання.
13. Тэрмін службы батарэі: Колькасць часу, калі акумулятар можа працягваць пастаўляць харчаванне пасля адзінай зарадкі.
14. Хуткая зарадка: Тэхналогія зарадкі, якая хутчэй забяспечвае харчаванне акумулятара, каб скараціць час зарадкі.
15. Сістэма кіравання акумулятарамі (BMS): Электрычная сістэма, якая адсочвае і кіруе станам батарэі, працэсам зарадкі і разгрузкі і абараняе батарэю ад неспрыяльных умоў, такіх як перанапружанне і перавышэнне зарадкі.
16. Жыццё цыкла батарэі: Колькасць цыклаў зарадкі, які батарэя можа запоўніць, звычайна вымяраецца зарадкай і разрадам на пэўную страту магутнасці, напрыклад, 80% ад першапачатковай магутнасці.
17. Максімальная стаўка платы: Максімальная хуткасць зарадкі, якую можна бяспечна прыняць акумулятарам, выражаецца як суадносіны магутнасці зарадкі.
18. Максімальная хуткасць разраду: Максімальная хуткасць току, з якой батарэю можна бяспечна выпісацца, выражаецца ў суадносінах току магутнасці.
19. Схема абароны батарэі: Прылада для бяспекі, якое выкарыстоўваецца для кантролю за станам батарэі і адключэння ланцуга батарэі ў выпадку перапланіроўкі, перавышэння, перанапружання, перавышанай і г.д., каб пазбегнуць пашкоджанняў або небяспекі для батарэі.
20. Палярнасць батарэі: Адрозненне і ідэнтыфікацыя паміж станоўчымі і адмоўнымі клемамі батарэі, як правіла, пазначаны сімваламі + і - або маркіроўкай.
21. Перапрацоўка батарэі: Працэс распараджэння выкарыстанымі батарэямі з мэтай аднаўлення і ўтылізацыі небяспечных матэрыялаў, якія змяшчаюцца ў іх, і паўторна выкарыстоўваць матэрыялы, якія падлягаюць утылізацыі.
22. Глыбокія вылучэнні: Умова, пры якім акумулятар выкідваецца на вельмі нізкі ўзровень альбо цалкам вычарпаны.Звычайна не рэкамендуецца глыбока разраду, каб пазбегнуць негатыўнага ўздзеяння на тэрмін службы батарэі.
23. Хуткі разрад: Тэхніка разраду, якая на кароткі прамежак часу выпускае энергію батарэі.
24. Збой батарэі: Умова, калі акумулятар не можа забяспечыць дастатковую магутнасць або падтрымліваць нармальную працу, што можа быць выклікана рознымі прычынамі, такімі як старэнне або пашкоджанне.
25. Цеплавы ўцёк : Ставіцца да хуткага і некантралюему павышэнню тэмпературы батарэі ў ненармальных умовах, такіх як перанапружанне, перагрэў і г.д.
26. Акумулятарныя электроды: Станоўчыя і адмоўныя электроды ў батарэі, якія з'яўляюцца ключавымі кампанентамі для захоўвання і вызвалення электрычнага зарада.
27. Станцыя па замене батарэі: Аб'ект або паслуга для хуткай замены батарэй у электрамабілях для забеспячэння большага дыяпазону.
28. Электрахімічная рэакцыя: Хімічная рэакцыя, якая адбываецца ў батарэі для пераўтварэння хімічнай энергіі ў электрычную энергію праз акісляльна -аднаўленчы працэс.
29. Электраліт: Праводная вадкасць або цвёрдая, якая выкарыстоўваецца для транспарціроўкі іёнаў паміж станоўчымі і адмоўнымі электродамі акумулятара, каб палегчыць электрахімічную рэакцыю.
30. Зарадная прылада: Прылада для перадачы электрычнай энергіі ў акумулятар для аднаўлення захаванай хімічнай энергіі.
31. Балансаванне акумулятара: Працэс, дзякуючы якому хуткасць зарадкі або разраду кожнай вочкі ў батарэі карэктуецца, каб гарантаваць, што зарад збалансаваны паміж асобнымі вочкамі.
32. Знешні акумулятар: Здымны акумулятар, які можа быць падлучаны да электроннага прылады для харчавання.
33. Індыкатар зарадкі акумулятара: Індыкатар або дысплей, які паказвае стан зарадкі або ўзровень батарэі.
34. Эфект памяці батарэі: З'ява, у выніку якой магутнасць батарэі паступова памяншаецца, паколькі цыклы зарадкі і разраду паўтараюцца, паколькі батарэя памятае меншы зарад і дыяпазоны разраду.
35. Непраходнасць: Ставіцца да ўнутранага супраціву батарэі, які ўплывае на эфектыўнасць і эфектыўнасць пераўтварэння энергіі.
36. Абарона тэмпературы: Функцыя або прылада, якая адсочвае і кантралюе тэмпературу батарэі, каб пазбегнуць перагрэву пашкоджанняў, калі тэмпература стане занадта высокай.
37. Абарона нізкага напружання: Механізм абароны, які аўтаматычна разразае ланцуг, каб прадухіліць празмерную разрыў, калі напружанне акумулятара апускаецца ніжэй бяспечнага парога.
38. Абарона зарадкі: Механізм абароны, які аўтаматычна адключае схему, каб прадухіліць перанаселенасць, калі зарад акумулятара дасягае парога бяспекі.
39. Захоўванне батарэі: Працэс утрымання батарэі ў нявыкарыстаным стане на працягу доўгага перыяду часу, часта патрабуючы адпаведных мер па зніжэнні самазарадка і абароны батарэі.
40. Сістэма кіравання акумулятарамі (BMS): Электронная сістэма маніторынгу, кантролю і абароны стану і прадукцыйнасці акумулятара, уключаючы кіраванне токам, напружаннем, тэмпературай і іншымі параметрамі.
41. Індыкатар узроўню батарэі: Прылада або функцыя, якая паказвае ўзровень зарадкі, які застаецца ў батарэі, звычайна выражаецца ў працэнтах альбо на некалькіх этапах.
42. Час зарадкі: Час, неабходны для прыцягнення батарэі ад нізкага зарадкі да поўнай зарадкі, на якую ўплывае магутнасць зараднай прылады і ёмістасць батарэі.
43. Каэфіцыент тэмпературы: Узаемасувязь паміж прадукцыйнасцю батарэі і зменамі тэмпературы, якія могуць паўплываць на магутнасць, унутранае супраціў і характарыстыкі зарадкі/разраду батарэі.
44. Гарантыя батарэі: Гарантыя вытворцы па прадукцыйнасці і якасці батарэі на працягу пэўнага перыяду часу, як правіла, выражаецца за некалькі месяцаў ці гадоў.
45. Станцыя падзарадкі: Абсталяванне або аб'ект, які выкарыстоўваецца для пастаўкі электрамабіляў або іншага абсталявання для зарадкі.
46. Тэстар батарэі: Прылада або прыбор, які выкарыстоўваецца для вымярэння напружання, ёмістасці, унутранага супраціву і іншых параметраў батарэі для ацэнкі яго здароўя і прадукцыйнасці.
47. Актыўнае балансаванне: Тэхніка кіравання акумулятарамі, якая раўняецца зарад у акумулятачнай батарэі, кантралюючы хуткасць зарадкі і разраду паміж асобнымі вочкамі.
48. Пасіўнае балансаванне: Тэхніка кіравання акумулятарамі, у якой зарад у батарэі збалансаваны шляхам падлучэння рэзістараў або ўцечкі зарадкі, звычайна менш эфектыўна, чым актыўнае балансаванне.
49. Упакоўка батарэі : Знешняя ўпакоўка акумулятара, якая выкарыстоўваецца для абароны клеткі, забяспечваюць структурную падтрымку і прадухіляе кароткія замыканні.
50. Шчыльнасць высокай энергіі: Максімальная колькасць электрычнай энергіі, якую акумулятар можа захоўваць на адзінку аб'ёму або вагі, што сведчыць аб эфектыўнасці захоўвання энергіі акумулятара.
51. Нізкая хуткасць самаадчування: Хуткасць, з якой батарэя губляе электрычную энергію самастойна, вельмі павольна і падтрымлівае высокі стан зарада пры захоўванні або нявыкарыстанні на працягу доўгага перыяду часу.
52. Палярызацыя батарэі: Ставіцца да змены матэрыялу на паверхні электродаў падчас зарадкі і разгрузкі з -за хімічных рэакцый на электродах.
53. Уцечка электраліта батарэі: Умова, пры якім электраліт у батарэі выцякае ў знешнюю сераду, што прывядзе да дэградацыі прадукцыйнасці батарэі ці іншых праблем бяспекі.
54. Сістэма астуджэння акумулятара: Сістэма, якая выкарыстоўваецца для кіравання тэмпературай батарэі альбо праз цеплавое рассейванне, вентылятар, альбо вадкае астуджэнне, каб захаваць батарэю ў адпаведным дыяпазоне працоўнай тэмпературы.
55. Сістэма ацяплення акумулятара: Сістэма, якая выкарыстоўваецца для забеспячэння цяпла батарэі ў асяроддзях з нізкай тэмпературай, каб забяспечыць належную працу батарэі пры нізкіх тэмпературах.
56. Акумулятар з высокай хуткасцю разраду: Акумулятар, які здольны дастаўляць электрычную энергію пры высокім току для прыкладанняў з высокімі патрабаваннямі магутнасці, такімі як электраінструменты і электрамабілі.
57. Другасная батарэя: Акумулятар, якую можна зарадзіць, у адрозненне ад аднаразовай батарэі, якая не папаўняецца.
58. Сачыце за батарэяй: Прылада або сістэма для маніторынгу стану, напружання, тэмпературы і іншых параметраў батарэі ў рэжыме рэальнага часу для прадастаўлення інфармацыі і абароны батарэі.
- Будаўніцтва батарэі: электроды, электраліт і сепаратар.
-
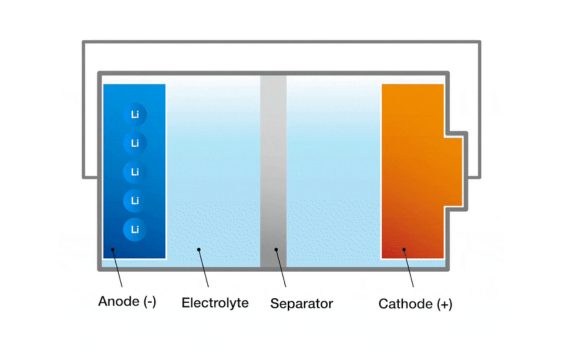
1. Электроды: Электроды ў батарэі дзеляцца на станоўчы і адмоўны электрод.Станоўчы электрод - гэта тое, дзе рэакцыя акіслення адбываецца ў батарэі, а адмоўны электрод - гэта тое, дзе ў батарэі адбываецца рэакцыя аднаўлення.Станоўчыя і адмоўныя электроды складаюцца з праводных матэрыялаў, звычайна металаў, вугляроду або злучэнняў.Розніца ў патэнцыяле паміж станоўчымі і адмоўнымі электродамі вырабляе напружанне акумулятара.
2. Электраліт: Электраліт - гэта асяроддзе паміж электродамі, што дазваляе іёнам праходзіць паміж электродамі і падтрымлівае баланс зарада.Электраліт можа быць у вадкай, цвёрдай або гель -форме, у залежнасці ад тыпу клеткі.У вадкай клеткі электраліт звычайна з'яўляецца іённым злучэннем, раствораным у растворы.
3. Дыяфрагма: Дыяфрагма - гэта фізічны бар'ер паміж станоўчымі і адмоўнымі электродамі, прадухіляючы прамы паток электронаў, але дазваляе іёнам праходзіць праз.Функцыя дыяфрагмы заключаецца ў прадухіленні кароткага замыкання станоўчых і адмоўных электродаў, дазваляючы іёнам свабодна перамяшчацца праз электраліт і падтрыманне балансу клеткі.Дыяфрагма звычайна вырабляецца з палімернага матэрыялу альбо керамічнага матэрыялу.
Гэтыя кампаненты працуюць разам, каб утварыць структуру батарэі.
- Працэсы зарада і разраду ў батарэях: хімічныя рэакцыі і паток току.
-
1. Працэс разраду: Калі акумулятар разраджаецца, хімічная энергія пераўтвараецца ў электрычную энергію.Падчас выпіскі рэакцыя акіслення адбываецца на станоўчым тэрмінале і рэакцыі аднаўлення на адмоўным тэрмінале.Хімічныя рэакцыі вырабляюць электроны і іёны.Станоўчы электрод вылучае электроны, якія паступаюць праз знешні ланцуг, каб атрымаць электрычны ток.Адмоўны электрод атрымлівае электроны, якія спалучаюцца з іёнамі, утвараючы злучэнні.У той жа час іёны перамяшчаюцца па электраліце, падтрымліваючы баланс зарадкі акумулятара.
2.Працэс зарадкі: Падчас зарадкі батарэі электрычная энергія пераўтвараецца ў хімічную энергію, каб захоўваць энергію.Падчас працэсу зарадкі знешняя крыніца харчавання прымяняе напружанне наперад, у выніку чаго ток праходзіць праз акумулятар.Станоўчае напружанне мяняе батарэю і мяняе хімічную рэакцыю паміж станоўчымі і адмоўнымі электродамі.Станоўчы электрод прымае электроны, а адмоўны электрод вызваляе іх.Хімічная рэакцыя захоўвае электрычную энергію ў якасці хімічнай патэнцыяльнай энергіі, аднаўляючы акумулятар у першапачатковым стане.Іёны перамяшчаюцца праз электраліт, каб падтрымліваць баланс зарадкі.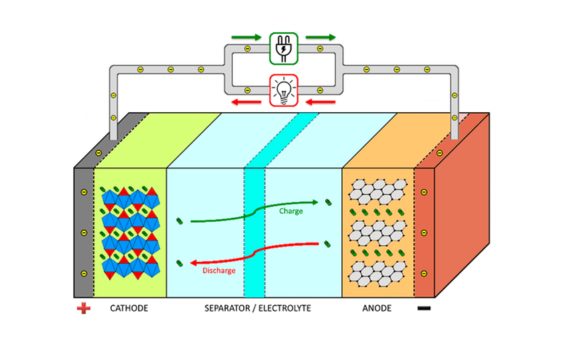
- Напружанне батарэі, ёмістасць і шчыльнасць энергіі.
-
Напружанне:
Напружанне - гэта паказчык трываласці электрычнага выхаду батарэі.Звычайна ён выражаецца ў вольтах.Агульныя напружання клетак акумулятара наступныя:
•Літый-іённы акумулятар (Li-Ion): звычайна 3,6 вольт да 3,7 вольт.Больш за тое, што батарэя LIFEPO4 (літый жалеза) складае 3,2 вольт.(Напружанне на адной клетках)
•Акумулятар нікеля-кадмію (NICD): 1,2 вольт (аднаклеткавае напружанне).
•NІкель-метал гідрыд (NIMH): 1,2 вольт (аднаклеткавае напружанне).
•Акумулятар свінцу-кіслот (свінцова-кіслата): ад 2 вольт да 2,2 вольт (напружанне з адзінкавым клеткам).Акумулятары свінцова-кіслот звычайна выкарыстоўваюцца ў аўтамабільных запуску, сістэмах захоўвання энергіі і іншых палёў.
•Цынк-шчолачны акумулятар (цынк-вуглярод): 1,5 вольт (аднаклеткавае напружанне).Гэты тып батарэі звычайна сустракаецца ў аднаразовых шчолачных батарэях, такіх як батарэі AA і AAA.
Вышэй прыведзены напружанне розных батарэй, і мы таксама можам павялічыць напружанне, злучаючы іх паслядоўна.Прыклады наступныя:
•Тры літый-іённыя батарэі 3,7 В падключаюцца паслядоўна, каб атрымаць 11.1V літый-іённы акумулятар (гэта значыць тое, што мы часта называем літый-іённым акумулятарам);
•Тры батарэі 2V-кіслоты падключаюцца паслядоўна, каб атрымаць 6V-кіслотны акумулятар;
• Чатыры батарэі фасфату 3,2 У літыевага жалеза падключаюцца, каб атрымаць 12,8 У літыевы жалезны фасфатны акумулятар (гэта значыць, што мы часта называем 12 В літый -фасфатнай батарэі)
Ёмістасць :
Калі казаць пра ёмістасць батарэі, ён часта выражаецца пры дапамозе адзінкі ампер (AH) або Milliampere-Hours (MAH).Ёмістасць акумулятара - гэта колькасць зарада, якую можа захоўваць акумулятар, і таксама можна зразумець як прадукт току і часу, які акумулятар можа даставіць.Вось некалькі прыкладаў лічбаў і спосабу іх апісання:
•Батарэя 2000 мАг: гэта азначае, што акумулятар мае ёмістасць 2000 мАг.Калі прылада прыцягвае сярэдні ток 200 міліампаў (MA) у гадзіну, то гэтая батарэя мож