راهنمای نهایی باتری ها
راهنمای زیر بسیار آموزنده است ، بنابراین بسته به سطح دانش باتری خود ، آنچه را که می خواهید از جدول مطالب بیاموزید ، پیدا کنید.البته اگر مبتدی هستید ، لطفاً از ابتدا شروع کنید.
نوک قبل از خواندن: یک بار روی کادر متن عنوان کلیک کنید و متن دقیق گسترش می یابد.دوباره کلیک کنید و متن مفصل پنهان خواهد شد.
معرفی
- اهمیت و کاربردهای گسترده باتری ها.
-
باتری ها در جامعه مدرن بسیار مهم هستند و در طیف گسترده ای از برنامه ها مورد استفاده قرار می گیرند (با توسعه فناوری ، دستگاه های بیشتر و بیشتر به باتری تبدیل می شوند).آنها راه حل های قابل حمل ، تجدید پذیر و اضطراری را ارائه می دهند که باعث توسعه فناوری ، استفاده از انرژی پایدار و پیشرفت در طیف گسترده ای از صنایع می شود.

1 دستگاه های الکترونیکی قابل حمل: مانند تلفن های همراه ، تبلت ، لپ تاپ و دوربین های دیجیتال.
2 حمل و نقل: وسایل نقلیه برقی و ترکیبی از باتری به عنوان دستگاه اصلی ذخیره انرژی استفاده می کنند.باتری ها با افزایش تقاضا برای انرژی های تجدید پذیر و شیوه های حمل و نقل سازگار با محیط زیست ، نقش مهمی در هدایت توسعه حمل و نقل پایدار دارند.
3 ذخیره انرژی تجدید پذیر: باتری ها به طور گسترده ای برای ذخیره منابع انرژی تجدید پذیر مانند انرژی خورشیدی و باد استفاده می شوند.با ذخیره انرژی الکتریکی در باتری ها ، آنها می توانند در صورت عدم دسترسی به انرژی خورشیدی یا باد ، برق ثابت برق را تأمین کنند.
4 قدرت اضطراری: باتری ها به عنوان منبع تغذیه پشتیبان در شرایط اضطراری نقش مهمی دارند.به عنوان مثال ، دستگاه هایی مانند تلفن های بی سیم ، مشعل و چراغ های اضطراری برای تأمین انرژی قابل اعتماد به باتری نیاز دارند.
5 تجهیزات پزشکی: بسیاری از دستگاه های پزشکی ، مانند ضربان سازها و دستگاههای تهویه مصنوعی ، از باتری ها به عنوان منبع تغذیه استفاده می کنند.ثبات و قابلیت اطمینان باتری ها برای عملکرد این دستگاه های مهم بسیار مهم است.
6 اقدامات نظامی: باتری ها در طیف گسترده ای از کاربردهای نظامی مانند تجهیزات ارتباطی نظامی ، سیستم های ناوبری و هواپیماهای بدون سرنشین استفاده می شوند.باتری ها می توانند یک منبع انرژی مستقل را فراهم کنند و قابلیت های جنگی را در میدان نبرد تقویت کنند.
7 صنعتی: باتری ها در صنعت برای سیستم های باتری ، منبع تغذیه اضطراری و سنسورهای بی سیم استفاده می شوند.آنها یک منبع تغذیه قابل اعتماد را فراهم می کنند و از تداوم و ایمنی تولید صنعتی اطمینان می دهند.
- مروری بر اصول اساسی و مکانیسم های کار باتری.
-
جادوی باتری ها در توانایی آنها در تبدیل انرژی شیمیایی به انرژی الکتریکی نهفته است.یک باتری شامل دو الکترود (مثبت و منفی) و یک الکترولیت است.الکترولیت به عنوان هادی یون ها عمل می کند و یک واکنش شیمیایی بین الکترودها را قادر می سازد.
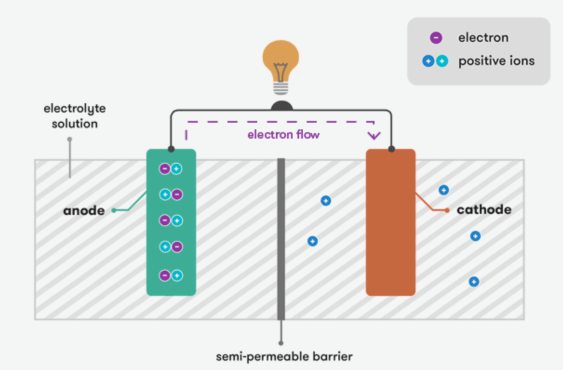
اصل اساسی یک باتری مبتنی بر واکنشهای الکتروشیمیایی است.هنگامی که یک واکنش شیمیایی رخ می دهد ، جریان الکترون ها را تولید می کند.در حالت شارژ ، باتری مواد شیمیایی بین الکترودهای مثبت و منفی را ذخیره می کند و واکنش شیمیایی برگشت پذیر است.هنگامی که باتری به یک مدار خارجی وصل شده است ، واکنش شیمیایی شروع می شود و باعث می شود مواد شیمیایی در ترمینال مثبت اکسید شوند و مواد شیمیایی در ترمینال منفی کاهش یابد.در نتیجه ، الکترون ها از ترمینال منفی به ترمینال مثبت جریان می یابند و جریان الکتریکی را تولید می کنند.این فرآیند تا زمانی که مواد شیمیایی از بین برود ادامه می یابد.
انواع مختلف باتری ها از واکنشهای شیمیایی متمایز برای تولید برق استفاده می کنند.به عنوان مثال ، متداول ترین نوع باتری لیتیوم یون: الکترود مثبت آن از یک ترکیب لیتیوم (مانند اکسید کبالت یا فسفات آهن لیتیوم) ساخته شده است و الکترود منفی آن از یک ماده کربن (مانند گرافیت) ساخته شده است.در حالت شارژ ، یون های لیتیوم از الکترود مثبت به مواد منفی تعبیه می شوند.در حین تخلیه ، یونهای لیتیوم از الکترود منفی تعبیه شده و به الکترود مثبت باز می گردند و الکترون ها را آزاد می کنند.
- ارزش داشتن یک راهنمای نهایی در مورد باتری ها برای خوانندگان.
-
یک راهنمای نهایی به دلایل مختلف برای خواننده ارزشمند است:
1 برای ارائه اطلاعات دقیق: اینترنت پر از قطعات اطلاعاتی و نظرات متناقض است.یک راهنمای نهایی با تثبیت و جمع آوری منابع معتبر ، اطلاعات جامع و دقیقی را ارائه می دهد تا به خوانندگان کمک کند تا به سرعت به دانش مورد نیاز خود دسترسی پیدا کنند و از اطلاعات گمراه کننده یا نادرست خودداری کنند.
2 صرفه جویی در وقت و تلاش: جستجو در اینترنت برای موضوعات خاص اغلب به زمان زیادی نیاز دارد تا از طریق و تأیید قابلیت اطمینان اطلاعات استفاده شود.راهنمای نهایی با جمع آوری اطلاعات مربوطه باعث صرفه جویی در وقت و تلاش می شود تا خوانندگان بتوانند تمام اطلاعات مورد نیاز خود را در یک مکان پیدا کنند.
3 حل تضادها و سردرگمی: اینترنت اغلب پاسخ های متفاوتی به همان سؤال یا تضاد بین اطلاعات ارائه می دهد.راهنمای نهایی به خوانندگان کمک می کند تا با سنتز دیدگاه های مختلف و منابع معتبر برای اطمینان از پاسخ های مختلف ، از سردرگمی و مبهوت فرار کنند.
4 راهنمایی و مشاوره ارائه دهید: راهنمای نهایی نه تنها حقایق و اطلاعات را ارائه می دهد ، بلکه می تواند راهنمایی و مشاوره عملی را نیز ارائه دهد.
- انواع مختلف باتری: اصول ، ویژگی ها و برنامه ها.
-
در اینجا برخی از 5 نوع متداول باتری از جمله اصول ، ویژگی ها و برنامه های کاربردی آنها آورده شده است.اگر می خواهید جامع ترین اطلاعات در مورد انواع باتری ، همچنین می توانید از این بخش پرش کنید و مستقیم به "بیشترین نوع باتری و برنامه های کاربردی" در زیر بروید.
باتری های اسید سرب
•اصل: باتری های اسید سرب از یک واکنش شیمیایی بین دی اکسید سرب و سرب برای تولید انرژی الکتریکی استفاده می کنند.
•ویژگی ها: کم هزینه ، جریان شروع بالا و چگالی انرژی ، اما بزرگ و سنگین.
•برنامه ها: باتری های استارت خودرو ، UPS (منبع تغذیه بدون وقفه) و غیره
باتری های لی-یون (لیتیوم یون)
•اصل: باتری های لیتیوم یون از مهاجرت یون های لیتیوم بین الکترودهای مثبت و منفی برای ذخیره و آزاد کردن انرژی الکتریکی استفاده می کنند.
•ویژگی ها: چگالی انرژی بالا ، وزن سبک تر و عمر چرخه طولانی تر.بازده شارژ بالا و تخلیه.
•برنامه ها: دستگاه های تلفن همراه (به عنوان مثال تلفن های همراه ، رایانه های لوحی) ، دستگاه های الکترونیکی قابل حمل و وسایل نقلیه برقی.
باتری های NICD (نیکل-کادمیوم)
•اصل: باتری های NICD از طریق واکنش شیمیایی بین نیکل و هیدروکسید کادمیوم ، انرژی الکتریکی تولید می کنند.
•ویژگی ها: تولید قدرت بالا و عمر طولانی ، اما آنها حاوی کادمیوم فلزی سنگین مضر هستند که تأثیر مشخصی بر محیط زیست دارد.
•برنامه ها: دوربین های دیجیتال ، ابزارهای قابل حمل و هواپیماهای بدون سرنشین و غیره
باتری های هیدرید NIMH (نیکل)
• اصل: باتری های NIMH از واکنش شیمیایی بین نیکل و هیدروژن برای ذخیره و آزاد کردن انرژی الکتریکی استفاده می کنند.
•ویژگی ها: چگالی انرژی بالا ، عمر طولانی ، آلودگی و عملکرد بهتر درجه حرارت بالا.
•برنامه ها: وسایل نقلیه ترکیبی ، سیستم های ذخیره انرژی و غیره
باتری لیپو (لیتیوم پلیمر)

•اصل: باتری لیتیوم پلیمر مشابه باتری لیتیوم یون است ، اما به جای الکترولیت مایع از یک الکترولیت پلیمری جامد استفاده می کند.
•ویژگی ها: چگالی انرژی بالا ، وزن سبک تر ، ایمنی بهتر و میزان تخلیه پایین تر.مناسب برای دستگاه های نازک.
•برنامه ها: لپ تاپ ، ساعتهای هوشمند و وسایل پزشکی قابل حمل و غیره
- دانش فیزیک باتری ها
- ولتاژ (v):
ولتاژ نشان دهنده اختلاف پتانسیل الکتریکی بین دو نقطه در یک مدار است.در ولت (V) اندازه گیری می شود.ولتاژ در سراسر باتری به طور معمول به عنوان V_BATT مشخص می شود.
شارژ (Q):
شارژ به میزان بار الکتریکی ذخیره شده در باتری اشاره دارد.در Coulombs (C) یا Ampere-Hours (AH) اندازه گیری می شود.رابطه بین شارژ و ظرفیت توسط: شارژ (Q) = ظرفیت (C) × ولتاژ (V)
ظرفیت (ج):
ظرفیت نشان دهنده میزان شارژ یک باتری است که می تواند ذخیره کند.به طور معمول در ساعتهای آمپر (AH) یا ساعت میلی لیتر (MAH) اندازه گیری می شود.رابطه بین ظرفیت ، بار و انرژی توسط: انرژی (E) = ظرفیت (C) × ولتاژ (V)
انرژی (ه):
انرژی ظرفیت انجام کار یا پتانسیل ایجاد یک سیستم برای ایجاد تغییرات است.در زمینه باتری ها ، انرژی اغلب در ساعتهای وات (WH) یا ژول (J) اندازه گیری می شود.رابطه بین انرژی ، ظرفیت و بار توسط: انرژی (E) = شارژ (Q) × ولتاژ (V)
قدرت (P):
قدرت نشان دهنده نرخ انجام کار یا انتقال انرژی است.در وات (W) اندازه گیری می شود.قدرت در یک مدار با استفاده از فرمول محاسبه می شود: قدرت (P) = ولتاژ (V) × جریان (I)
اتصال سری:
1. هنگامی که باتری ها به صورت سری وصل می شوند ، کل ولتاژ در سراسر مدار مجموع ولتاژهای باتری فردی است.جریان یکسان است.
ولتاژ کل (v_total) = v1 + v2 + v3 + ...
2. هنگامی که باتری ها به صورت سری به هم وصل می شوند ، ظرفیت کل مجموع ظرفیت های باتری فردی است.این امر به این دلیل است که جریان یکسان است ، اما کل ولتاژ افزایش می یابد.
ظرفیت کل (C_TOTAL) = C1 + C2 + C3 + ...
اتصال موازی:
1. هنگامی که باتری ها به صورت موازی به هم وصل می شوند ، کل ولتاژ همان باتری فردی باقی می ماند ، در حالی که کل جریان مجموع جریانهای موجود در هر باتری است.
کل جریان (i_total) = i1 + i2 + i3 + ...
2. هنگامی که باتری ها به صورت موازی متصل می شوند ، ظرفیت کل برابر با ظرفیت یک باتری واحد است.این امر به این دلیل است که ولتاژ یکسان است ، اما جریان کل افزایش می یابد.
ظرفیت کل (c_total) = c1 = c2 = c3 = ...
- شرایط و تعاریف باتری مشترک.
-
1 ظرفیت باتری: مقدار انرژی الکتریکی که یک باتری می تواند ذخیره کند ، که معمولاً در ساعت های آمپر (AH) یا Milli-Amps (MAH) بیان می شود.
2 ولتاژ: اختلاف بالقوه یا اختلاف ولتاژ باتری ، بیان شده در ولت V. نشان دهنده میزان انرژی الکتریکی است که باتری می تواند ذخیره کند.
3 سلول باتری: یک سلول فردی در باتری ، حاوی الکترود مثبت ، الکترود منفی و الکترولیت.
4 بسته باتری: یک کل متشکل از چندین سلول باتری ترکیبی.آنها معمولاً از طریق اتصالات ، تابلوهای مدار و سایر مؤلفه ها متصل و مدیریت می شوند.
5 اتصال سری: برای افزایش ولتاژ کل ، چندین سلول باتری که به ترتیب وصل شده اند ، با ترمینال مثبت به ترمینال منفی متصل می شوند.هنگامی که به صورت سری متصل می شوند ، ولتاژهای سلول قرار می گیرند.
6 اتصال موازی: چندین سلول باتری را به صورت توالی وصل می کند ، با ترمینال مثبت به ترمینال منفی ، برای افزایش توانایی و ظرفیت جریان کل.هنگامی که به طور موازی متصل می شوند ، ظرفیت سلولهای باتری به هم اضافه می شوند.
7 شارژ: تغذیه انرژی الکتریکی به باتری از یک منبع خارجی برای بازگرداندن انرژی شیمیایی ذخیره شده در باتری.
8 مرخصی: انتشار انرژی الکتریکی از باتری برای استفاده در تهیه تجهیزات الکترونیکی یا مدارها.
9 چرخه شارژ: به یک فرآیند شارژ کامل و تخلیه اشاره دارد.
10 راندمان هزینه: نسبت بین انرژی الکتریکی جذب شده توسط باتری و انرژی الکتریکی که در طی فرآیند شارژ ذخیره می شود.
11 خود را برآورده کردن: میزان باتری در هنگام استفاده از باتری به تنهایی قدرت خود را از دست می دهد.
12 عمر باتری: طول عمر یک باتری ، که معمولاً از نظر تعداد چرخه بار یا زمان استفاده اندازه گیری می شود.
13 عمر باتری: مدت زمانی که یک باتری می تواند پس از یک بار شارژ ، به تأمین انرژی خود ادامه دهد.
14 شارژ سریع: یک فناوری شارژ که برای کاهش زمان شارژ ، سریعتر باتری را به شما منتقل می کند.
15 سیستم مدیریت باتری (BMS): یک سیستم الکتریکی که وضعیت باتری ، فرآیند شارژ و تخلیه را کنترل و کنترل می کند و از باتری در برابر شرایط نامطلوب مانند بیش از حد و بیش از حد تخلیه محافظت می کند.
16 عمر چرخه باتری: تعداد چرخه های شارژ یک باتری می تواند تکمیل شود ، که معمولاً با شارژ و تخلیه به یک ظرفیت خاص از دست دادن ظرفیت خاص مانند 80 ٪ از ظرفیت اصلی اندازه گیری می شود.
17 حداکثر نرخ شارژ: حداکثر نرخ شارژ که می تواند با خیال راحت توسط باتری پذیرفته شود ، به عنوان نسبت ظرفیت بار بیان شده است.
18 حداکثر نرخ تخلیه: حداکثر نرخ جریان که در آن یک باتری با خیال راحت تخلیه می شود ، به عنوان نسبت ظرفیت جریان بیان می شود.
19. مدار حفاظت از باتری: یک دستگاه ایمنی که برای نظارت بر وضعیت باتری و جدا کردن مدار باتری در صورت شارژ بیش از حد ، بیش از حد ، بیش از حد ، جریان بیش از حد ، بیش از حد و غیره برای جلوگیری از آسیب یا خطر باتری استفاده می شود.
20 قطبیت باتری: تمایز و شناسایی بین پایانه های مثبت و منفی یک باتری ، که معمولاً توسط نمادها + و - یا مارک ها نشان داده می شود.
21 بازیافت باتری: فرآیند دفع باتری های استفاده شده به منظور بازیابی و دفع مواد خطرناک موجود در آنها و استفاده مجدد از مواد قابل بازیافت.
22. تخلیه عمیق: شرایطی که باتری در سطح بسیار کم تخلیه می شود یا کاملاً تخلیه می شود.تخلیه عمیق معمولاً به طور مکرر توصیه نمی شود تا از تأثیرات منفی بر عمر باتری جلوگیری شود.
23. ترشح سریع: یک روش تخلیه که انرژی باتری را برای مدت زمان کوتاهی در جریان بالا آزاد می کند.
24 خرابی باتری: شرایطی که باتری قادر به تأمین انرژی کافی یا حفظ عملکرد طبیعی نباشد ، که می تواند به دلایل مختلفی مانند پیری یا آسیب ایجاد شود.
25 فراری حرارتی : اشاره به افزایش سریع و غیرقابل کنترل دمای باتری در شرایط غیر طبیعی مانند شارژ بیش از حد ، بیش از حد ، گرمای بیش از حد و غیره است که ممکن است باعث انفجار باتری یا آتش سوزی شود.
26. الکترودهای باتری: الکترودهای مثبت و منفی در باتری ، که اجزای اصلی برای ذخیره و آزاد کردن بار الکتریکی هستند.
27. ایستگاه تعویض باتری: یک تسهیلات یا خدمات برای جایگزینی سریع باتری ها در وسایل نقلیه برقی برای تأمین محدوده طولانی تر.
28. واکنش الکتروشیمیایی: واکنش شیمیایی که در یک باتری برای تبدیل انرژی شیمیایی به انرژی الکتریکی از طریق یک فرآیند ردوکس صورت می گیرد.
29 الکترولیت: یک مایع رسانا یا جامد برای انتقال یون ها بین الکترودهای مثبت و منفی یک باتری برای تسهیل واکنش الکتروشیمیایی استفاده می شود.
30 شارژر: دستگاهی برای انتقال انرژی الکتریکی به باتری برای بازگرداندن انرژی شیمیایی ذخیره شده خود.
31. تعادل باتری: فرایندی که با استفاده از آن میزان شارژ یا تخلیه هر سلول در یک باتری تنظیم می شود تا اطمینان حاصل شود که بار بین سلولهای فردی متعادل است.
32 باتری خارجی: یک باتری قابل جابجایی که می تواند برای تأمین برق به یک دستگاه الکترونیکی وصل شود.
33 شاخص شارژ باتری: یک شاخص یا نمایشگر که وضعیت شارژ یا سطح باتری را نشان می دهد.
34 اثر حافظه باتری: پدیده ای که به موجب آن با تکرار چرخه بار و تخلیه ، ظرفیت باتری به تدریج کاهش می یابد ، زیرا باتری بار و تخلیه کوچکتر را به یاد می آورد.
35 امپدانس: اشاره به مقاومت داخلی یک باتری است که بر راندمان تبدیل انرژی و عملکرد آن تأثیر می گذارد.
36 حفاظت دما: عملکردی یا دستگاهی که در صورت افزایش درجه حرارت ، دمای باتری را کنترل و کنترل می کند.
37 محافظت از ولتاژ کم: مکانیسم حفاظت که به طور خودکار مدار را قطع می کند تا هنگام ولتاژ باتری در زیر آستانه ایمن ، از تخلیه بیش از حد جلوگیری کند.
38 محافظت بیش از حد: یک مکانیسم حفاظت که به طور خودکار مدار را قطع می کند تا هنگام رسیدن بار باتری به آستانه ایمنی از هزینه اضافی جلوگیری شود.
39 انباره باتری: فرآیند حفظ باتری در یک حالت بلااستفاده برای مدت طولانی ، که اغلب برای کاهش خود تخفیف و محافظت از باتری نیاز به اقدامات مناسب دارد.
40 سیستم مدیریت باتری (BMS): یک سیستم الکترونیکی برای نظارت ، کنترل و محافظت از وضعیت و عملکرد یک باتری از جمله مدیریت جریان ، ولتاژ ، دما و سایر پارامترها.
41 نشانگر سطح باتری: یک دستگاه یا عملکردی که نشان دهنده سطح بار باقی مانده در باتری است ، معمولاً به صورت درصد یا در چندین مرحله بیان می شود.
42 زمان شارژ: زمان لازم برای آوردن باتری از شارژ کم به شارژ کامل ، که تحت تأثیر قدرت شارژر و ظرفیت باتری است.
43 ضریب دمای: رابطه بین عملکرد باتری و تغییر دما ، که می تواند بر ظرفیت ، مقاومت داخلی و ویژگی های بار/تخلیه باتری تأثیر بگذارد.
44 ضمانت باتری: ضمانت یک تولید کننده در مورد عملکرد و کیفیت باتری برای مدت معینی ، معمولاً در ماه ها یا سالها بیان می شود.
45 ایستگاه شارژ: تجهیزات یا تسهیلات مورد استفاده برای تأمین وسایل نقلیه برقی یا سایر تجهیزات باتری برای شارژ.
46 تست کننده باتری: دستگاه یا ابزاری که برای اندازه گیری ولتاژ ، ظرفیت ، مقاومت داخلی و سایر پارامترهای یک باتری برای ارزیابی سلامت و عملکرد آن استفاده می شود.
47 تعادل فعال: یک روش مدیریت باتری که با کنترل میزان بار و میزان تخلیه بین سلولهای فردی ، بار در یک باتری را برابر می کند.
48 تعادل منفعل: یک روش مدیریت باتری که در آن شارژ در یک باتری با اتصال مقاومت یا نشت شارژ متعادل می شود ، معمولاً کمتر از تعادل فعال.
49 بسته بندی باتری : بسته بندی خارجی یک باتری ، که برای محافظت از سلول استفاده می شود ، پشتیبانی ساختاری و جلوگیری از مدارهای کوتاه را ارائه می دهد.
50 تراکم انرژی بالا: حداکثر مقدار انرژی الکتریکی که یک باتری می تواند در هر واحد حجم یا وزن آن را ذخیره کند ، و این نشانگر راندمان ذخیره انرژی باتری است.
51 نرخ پایین خود تخلیه: میزان از دست دادن باتری به تنهایی انرژی الکتریکی بسیار کند است و در هنگام ذخیره یا استفاده نشده برای مدت زمان طولانی از حالت شارژ بالایی برخوردار است.
52 قطبش باتری: به تغییر مواد موجود در سطح الکترودها در هنگام شارژ و تخلیه به دلیل واکنشهای شیمیایی روی الکترودها اشاره دارد.
53 نشت الکترولیت باتری: شرایطی که الکترولیت موجود در یک باتری به محیط خارجی نشت می کند ، که منجر به تخریب عملکرد باتری یا سایر مشکلات ایمنی خواهد شد.
54 سیستم خنک کننده باتری: سیستمی که برای کنترل دمای باتری ، یا از طریق اتلاف گرما ، فن یا خنک کننده مایع استفاده می شود تا باتری را در محدوده دمای کار مناسب نگه دارد.
55 سیستم گرمایشی باتری: سیستمی که برای تأمین گرما به باتری در محیط های دمای پایین برای اطمینان از عملکرد مناسب باتری در دماهای پایین استفاده می شود.
56 باتری با سرعت تخلیه بالا: باتری که قادر به ارائه انرژی الکتریکی در جریان بالا برای برنامه های کاربردی با نیازهای بالا مانند ابزارهای برق و وسایل نقلیه برقی است.
57 باتری ثانویه: باتری که قابل شارژ است ، بر خلاف باتری یکبار مصرف که قابل شارژ نیست.
58 مانیتور باتری: دستگاه یا سیستم برای نظارت بر وضعیت ، ولتاژ ، دما و سایر پارامترهای باتری در زمان واقعی برای ارائه اطلاعات و محافظت از باتری.
- ساخت باتری: الکترودها ، الکترولیت و جداکننده.
-
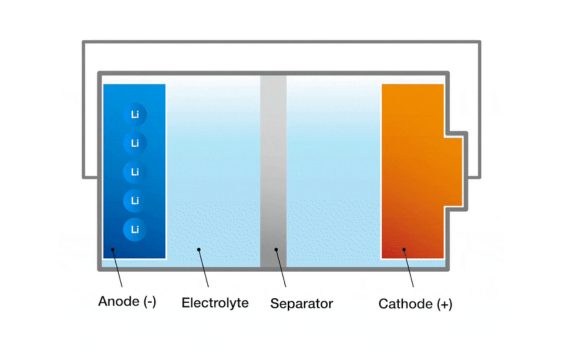
1 الکترودهای: الکترودهای موجود در باتری به یک الکترود مثبت و منفی تقسیم می شوند.الکترود مثبت جایی است که واکنش اکسیداسیون در باتری صورت می گیرد و الکترود منفی جایی است که واکنش کاهش در باتری صورت می گیرد.از الکترودهای مثبت و منفی از مواد رسانا تشکیل شده است ، معمولاً فلزات ، کربن یا ترکیبات استفاده می شود.تفاوت پتانسیل بین الکترودهای مثبت و منفی باعث ولتاژ سلول باتری می شود.
2 الکترولیت: الکترولیت واسطه بین الکترودها است که به یونها اجازه می دهد بین الکترودها عبور کنند و تعادل بار را حفظ کنند.این الکترولیت بسته به نوع سلول می تواند به صورت مایع ، جامد یا ژل باشد.در یک سلول مایع ، الکترولیت معمولاً یک ترکیب یونی است که در محلول حل می شود.
3 دیافراگم: دیافراگم یک مانع فیزیکی بین الکترودهای مثبت و منفی است و از جریان مستقیم الکترونی جلوگیری می کند اما اجازه می دهد یونها از آن عبور کنند.عملکرد دیافراگم جلوگیری از اتصال کوتاه الکترودهای مثبت و منفی در حالی که به یونها اجازه می دهد آزادانه از طریق الکترولیت حرکت کنند و تعادل بار سلول را حفظ کنند.دیافراگم معمولاً از یک ماده پلیمری یا یک ماده سرامیکی ساخته می شود.
این مؤلفه ها با هم کار می کنند تا ساختار سلول باتری را تشکیل دهند.
- فرآیندهای شارژ و تخلیه در باتری ها: واکنشهای شیمیایی و جریان جریان.
-
1 فرآیند تخلیه: هنگامی که باتری تخلیه می شود ، انرژی شیمیایی به انرژی الکتریکی تبدیل می شود.در حین ترخیص ، یک واکنش اکسیداسیون در ترمینال مثبت و یک واکنش کاهش در ترمینال منفی صورت می گیرد.واکنشهای شیمیایی الکترونها و یون ها را تولید می کنند.الکترود مثبت الکترون ها را آزاد می کند ، که از طریق یک مدار خارجی جریان می یابند تا جریان الکتریکی تولید کنند.الکترود منفی الکترون ها را دریافت می کند ، که با یون ها ترکیب می شوند تا ترکیبات تشکیل دهند.در عین حال ، یونها از طریق الکترولیت حرکت می کنند و تعادل بار باتری را حفظ می کنند.
2روند شارژ: در طی شارژ باتری ، انرژی الکتریکی به منظور ذخیره انرژی به انرژی شیمیایی تبدیل می شود.در طی فرآیند شارژ ، یک منبع تغذیه خارجی ولتاژ رو به جلو را اعمال می کند و باعث می شود جریان از باتری عبور کند.ولتاژ مثبت باتری را معکوس می کند و واکنش شیمیایی بین الکترودهای مثبت و منفی را معکوس می کند.الکترود مثبت الکترون ها را می پذیرد و الکترود منفی آنها را آزاد می کند.واکنش شیمیایی انرژی الکتریکی را به عنوان انرژی پتانسیل شیمیایی ذخیره می کند و باتری را به حالت اصلی خود باز می گرداند.یونها برای حفظ تعادل بار از طریق الکترولیت حرکت می کنند.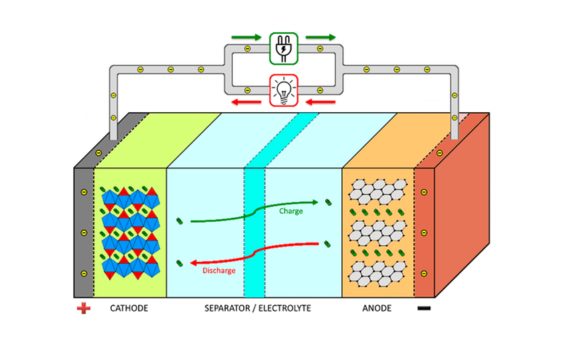
- ولتاژ باتری ، ظرفیت و چگالی انرژی.
-
ولتاژ:
ولتاژ اندازه گیری استحکام خروجی الکتریکی باتری است.معمولاً در ولت بیان می شود.ولتاژهای متداول باتری به شرح زیر است:
•باتری لیتیوم یون (Li-Ion): به طور کلی 3.6 ولت تا 3.7 ولت.نکته ویژه تر این است که باتری LifePO4 (لیتیوم آهن فسفات) 3.2 ولت است.(ولتاژ تک سلولی)
•باتری نیکل کادمیوم (NICD): 1.2 ولت (ولتاژ تک سلولی).
•حرفهیدرید ایکل فلزی (NIMH): 1.2 ولت (ولتاژ تک سلولی).
•باتری اسید سرب (اسید سرب): 2 ولت تا 2.2 ولت (ولتاژ تک سلولی).باتری های اسید سرب معمولاً در شروع خودرو ، سیستم های ذخیره انرژی و سایر زمینه ها مورد استفاده قرار می گیرند.
•باتری روی-آلکالین (روی-کربن): 1.5 ولت (ولتاژ تک سلولی).این نوع باتری معمولاً در باتری های قلیایی یکبار مصرف مانند باتری های AA و AAA یافت می شود.
موارد فوق ولتاژ باتری های مختلف است و همچنین می توانیم با اتصال آنها به صورت سری ولتاژ را افزایش دهیم.مثالها به شرح زیر است:
•سه باتری لیتیوم 3.7 ولت به صورت سری به هم متصل می شوند تا یک باتری لیتیوم یون 11.1 ولت را بدست آورند (یعنی چیزی که ما اغلب آن را یک باتری لیتیوم یون 12 ولت می نامیم).
•سه باتری اسید سرب 2 ولت به صورت سری به هم وصل می شوند تا یک باتری اسید سرب 6 ولت دریافت کنند.
• چهار باتری فسفات آهن لیتیوم 3.2 ولت به صورت سری به هم وصل می شوند تا یک باتری فسفات آهن 12.8 ولت لیتیوم را بدست آورند (یعنی آنچه که ما اغلب آن را یک باتری فسفات آهن لیتیوم 12 ولت می نامیم)
ظرفیت:
هنگام صحبت در مورد ظرفیت باتری ، اغلب با استفاده از واحد Ampere-Hours (AH) یا Milliampere ساعت (MAH) بیان می شود.ظرفیت باتری مقدار شارژ است که یک باتری می تواند ذخیره کند و همچنین می تواند به عنوان محصول فعلی و زمانی که باتری می تواند تحویل دهد درک شود.در اینجا چند شکل مثال و نحوه توصیف آنها آورده شده است:
•باتری 2000 میلی آمپر ساعت: این بدان معنی است که باتری دارای ظرفیت 2000 میلی آمپر ساعت است.اگر دستگاه به طور متوسط جریان 200 میلی ثانیه (MA) در ساعت را ترسیم کند ، این باتری می تواند از نظر تئوری 10 ساعت (2000mAh / 200mA = 10 ساعت) تأمین کند.
•باتری 5AH: این بدان معنی است که باتری ظرفیت 5 آمپر ساعت دارد.اگر دستگاه جریان متوسط 1 آمپر (الف) در ساعت را مصرف کند ، این باتری از نظر تئوریک می تواند به مدت 5 ساعت (5AH / 1A = 5 ساعت) قدرت یابد.
بسته های باتری را می توان به طور موازی به هم وصل کرد تا ظرفیت بیشتری داشته باشد ، به عنوان مثال:
•2 باتری لیتون یون از 12V-100AH را می توان به طور موازی برای تهیه یک باتری LI-Ion از 12V-200AH به هم وصل کرد.
•2 باتری LifePO4 از 3.2V-10AH می تواند به طور موازی وصل شود تا یک باتری LifePo4 از 3.2V-20AH دریافت کند.
شارژر باتری 1000mAh: این یک شارژر است که می تواند باتری را با سرعت 1000 میلی لیتر (MA) در ساعت شارژ کند.اگر باتری 2000 میلی آمپر ساعتی داشته باشید ، شارژ آن با این شارژر از نظر تئوری 2 ساعت (2000mAh / 1000mA = 2 ساعت) طول می کشد تا آن را به طور کامل شارژ کند.
در عمل ، زمان استفاده از باتری محاسبه شده از نظر تئوری ممکن است به دلیل سایش باتری و پارگی و سایر عوامل منحرف شود.
تراکم انرژی:
چگالی انرژی اندازه گیری کارآیی انرژی ذخیره شده در یک باتری است.این نشان می دهد میزان انرژی قابل ذخیره در هر واحد حجم یا وزن واحد باتری.واحدهای متداول چگالی انرژی وات ساعت در هر کیلوگرم (WH/kg) یا وات ساعت در لیتر (WH/L) است.
•باتری لیتیوم یون: باتری های لیتیوم یون دارای چگالی انرژی بالایی هستند ، به طور معمول از 150 تا 250 WH/kg.
•باتری NIMH: باتری های NIMH در مقایسه با باتری های لیتیوم یون چگالی انرژی کمتری دارند.آنها به طور معمول از 60 تا 120 WH/kg است.
•باتری اسید سرب: باتری های اسید سرب در مقایسه با باتری های لیتیوم یون ، چگالی انرژی نسبتاً کمی دارند.آنها به طور معمول از 30 تا 50 WH/kg است.
•باتری روی-کربن: باتری های کربن روی در مقایسه با باتری های لیتیوم یون ، چگالی انرژی کمتری دارند.آنها به طور معمول از 25 تا 40 WH/kg است.
- توصیه های ذخیره باتری
-
ذخیره مناسب باتری برای حفظ سلامت باتری و طولانی شدن طول عمر آن ضروری است.در اینجا چند توصیه برای ذخیره باتری ها آورده شده است:
•دما: باتری ها را در یک مکان خنک و خشک با دمای بین 15 درجه سانتیگراد و 25 درجه سانتیگراد (59 درجه فارنهایت و 77 درجه فارنهایت) ذخیره کنید.درجه حرارت بالا می تواند سرعت خود را تسریع کرده و ماندگاری باتری را کوتاه کند.از قرار گرفتن باتری ها در گرمای شدید یا سرماخوردگی خودداری کنید.
•از رطوبت خودداری کنید: رطوبت می تواند به باتری ها آسیب برساند و منجر به خوردگی یا نشت شود.باتری ها را از محیط های مرطوب مانند زیرزمین یا حمام دور نگه دارید.اطمینان حاصل کنید که محل نگهداری خشک و تهویه مناسب است.
•سطح شارژ: قبل از ذخیره باتری برای مدت طولانی ، بهتر است اطمینان حاصل شود که آنها تا حدی شارژ شده اند.بیشتر تولید کنندگان برای ذخیره طولانی مدت میزان شارژ حدود 40 تا 60 ٪ را توصیه می کنند.این محدوده به جلوگیری از هزینه بیش از حد یا هزینه بیش از حد در هنگام ذخیره کمک می کند.
•نوع باتری: شیمیایی های مختلف باتری دارای نیازهای خاص برای ذخیره سازی هستند.در اینجا چند دستورالعمل برای انواع مشترک وجود دارد:
آ. باتری های قلیایی: باتری های قلیایی ماندگاری طولانی دارند و می توانند برای چندین سال ذخیره شوند.آنها قابل شارژ نیستند و نباید در معرض دمای شدید قرار بگیرند.
ب. باتری های لیتیوم یون: باتری های Li-ion که معمولاً الکترونیک قابل حمل است.اگر قصد دارید آنها را برای مدت طولانی ذخیره کنید ، هدف خود را بین 40 تا 60 ٪ هدف قرار دهید.از ذخیره باتری های Li-ion با شارژ کامل یا به طور کامل تخلیه خودداری کنید.
ج. باتری های اسید سرب: اینها معمولاً در وسایل نقلیه و سیستم های پشتیبان تهیه می شوند.برای ذخیره طولانی مدت ، باتری های اسید سرب را به طور کامل شارژ کنید.به طور مرتب سطح الکترولیت را بررسی کرده و در صورت لزوم با آب مقطر بالا بروید.
د. <